Общая информация
Краткое описание
Коды по МКБ 10:
Q 68.3 Врожденное искривление бедра
Q 68.4 Врожденное искривление костей голени
М 21.0 Приобретенная вальгусная деформация конечности
М 21.1 Приобретенная варусная деформация конечности
М 21.9 Приобретенная деформация конечности неуточненная
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
1. Вальгусная деформация.
2. Варусная деформация.
3. Антекурвационная деформация.
4. Рекурвационная деформация.
Диагностика
Диагностические критерии
Жалобы и анамнез: в анамнезе при врожденной патологии в возрасте 1-1,5 лет выявляется деформация конечности, появляется прихрамывание, позднее боли в суставах после длительной ходьбы. При приобретенной патологии деформация конечности появляется после снятия гипсовой иммобилизации или в ближайшее время после нагрузки.
Физикальное обследование: нарушение походки (хромота или прихрамывание), выраженная осевая деформация конечности, ограничение движений в близлежащем суставе.
Лабораторные исследования: изменений в клинических, биохимических анализах при отсутствии сопутствующей патологии не наблюдается.
Инструментальные исследования: на рентгенограммах костей в двух проекциях отмечается осевая деформация костей.
Минимум обследования при направлении в стационар:
3. Анализ на ВИЧ, гепатиты в случае перенесенных ранее оперативных вмешательств.
Основные диагностические мероприятия:
1. Общий анализ крови (6 параметров), гематокрит, тромбоциты, свертываемость.
2. Определение остаточного азота, мочевины, общего белка, билирубина, кальция, калия, натрия, глюкозы, АЛТ, АСТ.
3. Определение группы крови и резус-фактора.
4. Общий анализ мочи.
5. Рентгенография тазобедренных суставов в прямой проекции и с внутренней ротацией.
6. УЗИ органов брюшной полости.
9. ИФА на маркеры гепатитов В, С, Д, ВИЧ по показаниям.
10. ЭМГ по показаниям.
Дополнительные диагностические мероприятия:
1. Анализ мочи по Аддису-Каковскому по показаниям.
2. Анализ мочи по Зимницкому по показаниям.
3. Посев мочи с отбором колоний по показаниям.
4. Рентгенография грудной клетки по показаниям.
5. ЭхоКГ по показаниям.
Дифференциальный диагноз
Признак
Деформация конечностей
Фиброзная дисплазия
Незавершенный остеогенез
Начало появления деформации
В раннем детстве или после травмы
Постепенное проявление деформации
Варусные, вальгусные, рекурвационные, антекурвационные
Сложные осевые и комбинированные
Сложные осевые и комбинированные
Структура кости не изменена
Истончение кортикального слоя, наличие очагов
Атрофия диафизов, прозрачность костной ткани
Лечение
Тактика лечения
Цели лечения: устранение осевой деформации конечности, статической боли в суставах путем корригирующих остеотомий с наложением аппаратов ЧКО или металло-остеосинтезом.
Медикаментозное лечение:
3. Обезболивающая терапия в послеоперационном периоде с первых суток (трамадол, кетонал, триган, промедол) по показаниям, в течение 3-5 суток.
5. С целью профилактики гипокальциемии (глюконат кальция, кальций-Дз Никомед, кальцид, остеогенон) перорально с 7-10 суток после операции, в возрастной дозировке.
Переливание компонентов крови (СЗП, эрмасса одногруппная) интраоперационно и в послеоперационном периоде по показаниям.
Профилактические мероприятия: профилактика бактериальной и вирусной инфекции.
1. Профилактика контрактур и тугоподвижности сустава.
2. Профилактика остеопороза.
Основные медикаменты:
5. Препараты кальция в таблетках
Дополнительные медикаменты:
1. Препараты железа перорально
2. Растворы глюкозы в\в
3. Раствор NaCl 0,9% в\в
5. Металлоконструкции и аппараты ЧКО
Индикаторы эффективности лечения:
1. Устранение осевой деформации конечности.
2. Восстановление полного объема движений в суставах.
Госпитализация
Показания к госпитализации: плановое, выраженная осевая деформация костей верхних и нижних конечностей с нарушением функции конечности в виде хромоты, ограничения функции сустава, боли в близлежащих суставах.
Дефект предсердной перегородки
Рубрика МКБ-10: Q21.1
Содержание
Определение и общие сведения [ править ]
По эмбриологическому генезу, т.е. в зависимости от характера и степени недоразвития первичной и вторичной межпредсердных перегородок и эндокардиальных валиков, выделяют первичные, вторичные дефекты и полное отсутствие МПП (единственное, общее предсердие, трехкамерное сердце).
Единственное (общее) предсердие формируется в результате недоразвития в эмбриональном периоде или полного отсутствия первичной и вторичной МПП и наличия большого дефекта, равного по площади всей МПП. При этом сохранены два предсердных ушка и дифференциальная структура правой и левой стенок предсердия. Поскольку нарушено развитие первичной МПП и эндокардиальных валиков, порок, как правило, сочетается с дефектом формирования атриовентрикулярных клапанов, поэтому может рассматриваться как одна из форм ОАВК. При данном пороке нередко наблюдается аспления.
Дефекты МПП могут быть также комбинированными (первичный и вторичный ДМПП или в сочетании с дефектом венозного синуса).
Этиология и патогенез [ править ]
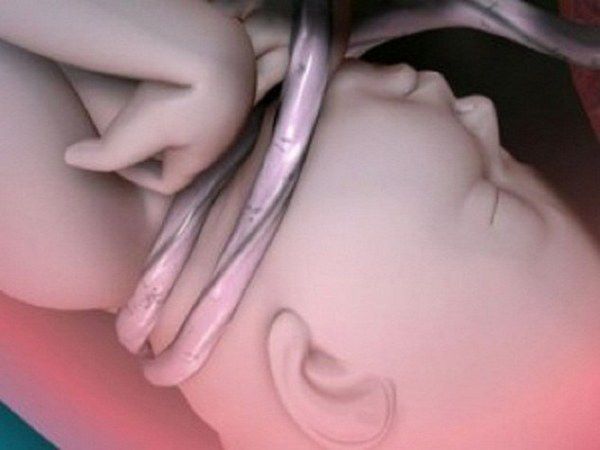
Гемодинамика. Во внутриутробном периоде развития наличие межпредсердного сообщения не является аномальным и не оказывает патологического влияния на гемодинамику плода.
В основе гемодинамических нарушений, возникающих после рождения, лежит артериовенозный сброс крови из левого предсердия в правое, обусловленный не только положительным градиентом давления между левым (6-8/0-1 мм рт.ст.) и правым (4-5/0-1 мм рт. ст.) предсердиями, но и большей физиологической растяжимостью и податливостью (комплайнсом) правого предсердия и правого желудочка, большим диаметром правого венозного устья в сравнении с соответствующими отделами левой половины сердца. Кроме того, кровь из правых отделов сердца изгоняется в систему легочной артерии, давление в которой (20-30/8-10 мм рт.ст.) почти в 4 раза ниже системного АД (80-120/60-80 мм рт.ст.). Поэтому величина сброса зависит как от размеров (площади) дефекта (5-30 мм), так и от соотношения степени гипертрофии и толщины стенок левых и правых камер сердца, а также от величин давления в легочной артерии и аорте. При этом градиент давления между предсердиями влияет на величину сброса лишь при небольших дефектах (до 1-2 см), а при больших дефектах (более 2-3 см) давление между предсердиями выравнивается (исчезает межпредсердный градиент) и величина сброса, а позже и направление шунта обусловлены исключительно соотношением величин комплайнса правых и левых камер сердца и сосудистых сопротивлений в МКК (малый круг кровообращения) и БКК (большой круг кровообращения).
У новорожденных и детей первых месяцев жизни до возникновения выраженного физиологического преобладания левых отделов сердца давление в легочной артерии относительно высокое (30-35 мм рт.ст.), а системное АД низкое, поэтому артериовенозный сброс небольшой и существенных гемодинамических нарушений нет. В первые недели жизни при кратковременной задержке дыхания и повышении сопротивления в МКК (сосание, крик, плач, натуживание, дефекация и др.) даже возможен кратковременный веноартериальный сброс в левое предсердие с возникновением слабого транзиторного цианоза. Это наиболее часто наблюдается при дефектах, расположенных около устьев полых вен.
По мере взросления ребенка и усиления его двигательной активности в ортостазе увеличивается прирост системного АД и возникает физиологическое доминирование левых отделов сердца, вследствие чего артериовенозный сброс постепенно увеличивается. Это приводит к увеличению «балластного» объема крови, циркулирующего через МКК, его гиперволемии (обогащению). Величина артериовенозного сброса при ДМПП достигает 10-15 л/мин.
Длительная объемная перегрузка правых камер сердца приводит к их дилатации и умеренной гипертрофии, поскольку сопротивление кровотоку небольшое из-за значительной депонирующей способности МКК («сосудистого ложа» легкого) и низкой резистивности сосудов легочного русла. Лишь когда легочный кровоток превышает норму в 3 раза, возникает умеренная легочная гипертензия (в пределах 35-40 мм рт.ст.) гиперкинетического типа.
Если легочная гипертензия у пациента развилась, это, как правило, является признаком склеротической стадии, и потому прогноз заболевания хуже. Выявление при ДМПП ранней прогрессирующей легочной гипертензии необходимо, вероятно, расценивать как сопутствующую задержку фетальной инволюции легочных сосудов. Возрастающая легочная гипертензия добавляет к объемной, диастолической перегрузке правых отделов сердца и систолическую перегрузку сопротивлением, что приводит к еще большей гипертрофии правого желудочка. Легочная артерия иногда расширяется, и также дилатируется перегруженное объемом левое предсердие. Однако его гипертрофия выражена умеренно, так как кровь из устьев правых легочных вен почти непосредственно впадает в правое предсердие. Из-за увеличения легочного сопротивления и снижения растяжимости гипертрофированных утолщенных стенок правого желудочка в нем возрастает конечное диастолическое давление, среднее давление повышается в гипертрофированном правом предсердии. В результате происходит «смена шунта» с возникновением вначале транзиторного веноартериального сброса (при физической нагрузке, спастическом кашле, натуживании и др.), а затем и стойкого, при котором цианоз отмечается в покое постоянно.
Характерно для данного состояния расширения ствола легочной артерии на фоне формирования относительного функционального стеноза нормального отверстия легочного клапана, размеры которого не соответствуют уже значительно возросшему ударному объему правого желудочка.
В поздних стадиях развития порока (во II-III декаде жизни) происходит «изнашивание» (дистрофия, склероз) миокарда правого желудочка и развивается сначала правожелудочковая, а затем и тотальная сердечная недостаточность, при этом веноартериальный сброс значительно снижается.
Клинические проявления [ править ]
Клинически ДМПП относится к гемодинамически длительно компенсированным и маломанифестным порокам. Выраженность его симптоматики зависит от величины и локализации дефекта, а также в большей степени от длительности существования порока и развития вторичных осложнений.
До 2-5 лет клиническая симптоматика порока очень скудная, поэтому в младшем возрасте порок выявляют редко или расценивают как функциональную кардиопатию (возможное появление в периоде новорожденности транзиторного цианоза при крике и беспокойстве чаще связывают с перинатальной энцефалопатией).
Дети с небольшой величиной дефекта (до 10-15 мм) развиваются нормально, удовлетворительно переносят нагрузки, первые симптомы порока могут появляться у них лишь во втором десятилетии жизни. Несмотря на постоянную бледность, наличие цианоза нехарактерно для детей с ДМПП, так как легочная гипертензия и сердечная недостаточность у них чаще формируются лишь к 20 годам.
АД нормальное, а при больших дефектах снижается максимальное и пульсовое АД. Пульс нормального напряжения и несколько пониженного наполнения.
Границы сердца увеличены вправо и вверх за счет предсердий, но при больших дефектах и в старшем возрасте отмечается также расширение левой границы сердца, как правило, за счет правого желудочка, оттесняющего левый желудочек кзади. Выраженная кардиомегалия возникает редко.
В поздних стадиях заболевания при значительном расширении ствола легочной артерии (у 10-35% больных) иногда появляется нежный протодиастолический шум относительной недостаточности пульмонального клапана (шум Грехема-Стилла).
Дефект предсердной перегородки: Диагностика [ править ]
Фонокардиография. I тон в 5 ЛСК и 3-4 ЛС, как правило, увеличен по амплитуде, иногда расщеплен до 0,02-0,03 сек. II тон в 2 ЛС раздвоен (более 0,03 сек.) с возрастанием амплитуды пульмонального компонента. В 3-4 ЛС в диастоле может регистрироваться низко- и среднеамплитудный III тон, связанный с быстрым наполнением правого желудочка, и 4-й пресистолический экстратон, обусловленный сильным сокращением правого предсердия. В 2 ЛС и 3-4 ЛС фиксируется среднечастотный среднеамплитудный систолический шум, чаще ромбовидной или веретенообразной формы, на 1 /2— 2 /3 систолы. По мере нарастания легочной гипертензии III тон уменьшается, а II и IV тоны увеличиваются по амплитуде, при этом исчезает раздвоение II тона. Это связано с более ранним и быстрым закрытием пульмонального клапана и приближением пульмонального компонента к аортальному. Шум Грехема-Стилла записывается как высокочастотный низкоамплитудный протодиастолический шум, лучше фиксируемый в 2 ЛС и 3-4 ЛС.
Катетеризация сердца и ангиокардиография. Совершенствование и широкое внедрение в клиническую практику такого неинвазивного метода, как эхокардиография, сузило показания к использованию катетеризационных методов обследования детей с ВПС.
О наличии ДМПП свидетельствуют возможность прохождения зонда из правого предсердия в левое, более высокое насыщение кислородом крови, взятой из полости правого предсердия, по сравнению с пробами крови, взятой около устьев полых вен. Разница в10% и более считается абсолютным признаком артериовенозного шунта крови.
Давление в правом предсердии, правом желудочке и легочной артерии умеренно повышено, однако в детском возрасте оно очень редко превышает 45-50 мм рт.ст. Несмотря на функциональный характер стеноза, систолический градиент между давлением в правом желудочке и легочной артерии достигает 30 мм рт.ст.
Дифференциальный диагноз [ править ]
Дифференциальную диагностику ДМПП с большим сбросом следует проводить с:
• ВПС, протекающими с обогащением МКК;
• умеренным изолированным СЛА.
При малых вторичных ДМПП необходимо проводить дифференциальную диагностику с функциональной кардиопатией и нейроциркуляторной дистонией.
Дефект предсердной перегородки: Лечение [ править ]
Естественное течение порока и прогноз определяются размером дефекта и величиной артериовенозного сброса. Дети с вторичными ДМПП и малым сбросом крови развиваются нормально, не предъявляют жалоб, многие годы у них сохраняется физическая работоспособность, а первые симптомы неблагополучия иногда выявляются лишь в третьем десятилетии жизни. Однако в дальнейшем заболевание быстро прогрессирует, и большая часть пациентов умирают в возрасте до 40 лет, а живущие к 50 годам становятся инвалидами. Тем не менее часто описывают случаи, когда больные с вторичным ДМПП доживали до 70-80 лет. У некоторых пациентов с небольшим ДМПП происходит спонтанное закрытие дефекта в течение первых 2-5 лет жизни.
Младенческая смертность в основном обусловлена первичным ДМПП и (или) наличием ДМПП и АДЛВ, дефектов атриовентрикулярных клапанов, а также сочетанием ДМПП с экстракардиальными врожденными аномалиями. Непосредственными причинами смерти чаще всего являются тяжелые вирусные инфекции, рецидивирующие пневмонии, кишечные инфекции.
Больным, у которых уже имеется очерченная клиническая симптоматика, подтвержденная инструментально и рентгенологически, показано оперативное вмешательство. Современная тенденция предусматривает раннюю хирургическую коррекцию ВПС, но часто имеется возможность отложить операцию на более поздний срок, когда риск от ее проведения уменьшается. У детей при условии эффективности консервативного лечения порока операцию можно отложить до 3-5-летнего возраста, однако если консервативное лечение малоэффективно, то операция показана всем больным, независимо от их возраста.
Наиболее частыми причинами летальных исходов являются острая сердечная недостаточность, эмболия и гипоксические поражения головного мозга.
Профилактика [ править ]
Прочее [ править ]
Открытое овальное отверстие также является вариантом межпредсердной коммуникации и может быть обусловлено как недоразвитием клапана овального отверстия, так и его дефектом. Необходимо отметить, что открытое овальное отверстие не относится к истинным дефектам перегородки, обусловленным недостаточностью ее ткани, поэтому не может быть причислено к ДМПП.
Что такое перинатальная энцефалопатия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Гавриловой Татьяны Алексеевны, детского невролога со стажем в 20 лет.
Определение болезни. Причины заболевания
Перинатальная энцефалопатия (перинатальное поражение центральной нервной системы) — это заболевание, которое характеризуется повреждением нервной системы ребёнка в перинатальный период.
Перинатальная энцефалопатия (ПЭП) и перинатальное поражение ЦНС — это равнозначные термины, однако детские неврологи чаще применяют второй вариант при постановке диагноза.
В РФ принято объединять всевозможные варианты поражения нервной системы под одним общим диагнозом – «перинатальная энцефалопатия», а в международной классификации, наоборот, максимально уточнять его название и код.
То есть российскому обобщённому диагнозу «перинатальная энцефалопатия» в МКБ-10 может соответствовать несколько уточнённых диагнозов, например:
Основные факторы, приводящие к повреждению нервной системы во время беременности:
Основные факторы, приводящие к повреждению нервной системы в родах:
Основные факторы, приводящие к повреждению головного мозга после родов:
Симптомы перинатальной энцефалопатии
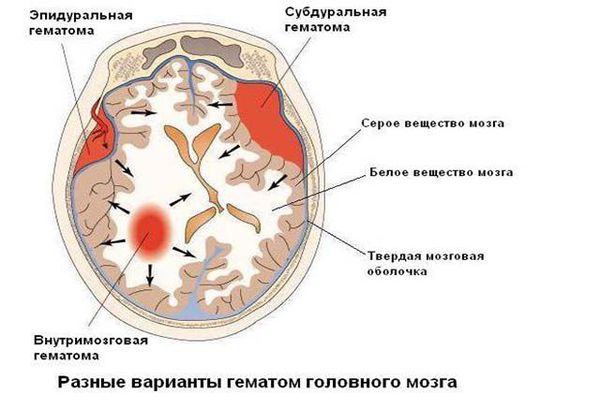
Уже при рождении при наличии тяжёлой родовой травмы с внутричерепным или внутрижелудочковым кровоизлиянием, асфиксией в родах и т. д. у детей отмечаются такие проявления, как угнетение или возбуждение ЦНС, внутричерепная гипертензия (повышенное давление), судороги и даже кома. В таком случае дети экстренно госпитализируются в отделение неонатологии, где получают интенсивное лечение под постоянным наблюдением врачей с внутривенным введением лекарственных препаратов. При необходимости детей временно подключают к аппарату ИВЛ (искусственной вентиляции лёгких).
У детей до года с перинатальной энцефалопатией клинические проявления делят на несколько групп.
Синдром двигательных нарушений:
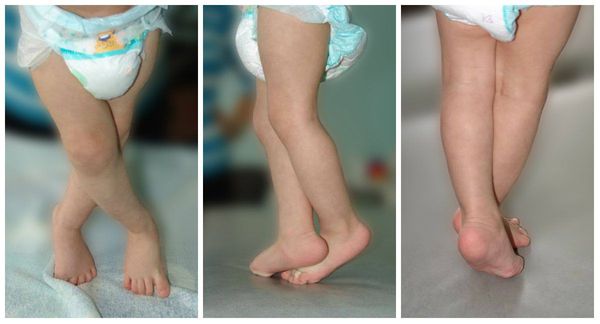
Мышечный тонус при этом может быть повышен либо снижен. При повышении тонуса мышц в руках преобладает тонус в сгибателях (ребёнок держит ручки в кулачках), в ногах преобладает тонус в икроножных мышцах и приводящей группе мышц бедра (при попытке поставить на поверхность ребёнок поджимает пальцы стоп, опора на носочки с перекрёстом).
Также у многих детей с перинатальным поражением ЦНС отмечается задержка психомоторного развития. В связи с чем детский невролог должен чётко знать календарь психомоторного развития у детей до года. При нормальном психомоторном развитии дети начинают:
Существуют индивидуальные особенности развития, небольшие отклонения в развитии могут проходить самостоятельно, но отставание в психомоторном развитии доношенного ребёнка на 2 месяца и более требует осмотра детского невролога для решения вопроса: нуждается ли ребёнок в лечении и назначении комплексной реабилитации.
Не стоит заниматься самолечением, обследование и лечение ребёнку должен назначить детский невролог.
Патогенез перинатальной энцефалопатии
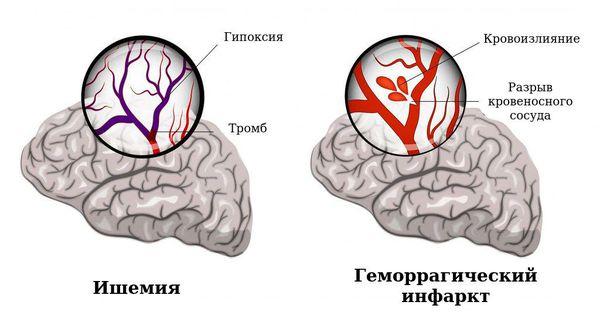
При неблагополучном течении беременности и родов универсальным патогенетическим фактором, повреждающим головной мозг, является гипоксия — это недостаточное поступление кислорода к клеткам головного мозга.
Существует два основных варианта повреждения головного мозга:
Поражение нервной системы при внутриутробных инфекциях сопровождается вовлечением в воспалительный процесс тканей головного мозга и его оболочек (энцефалит, менингит), повышением внутричерепного давления и присоединением судорог.
Возможен также механический перелом ключицы, с повреждением нервного сплетения, расположенного вблизи, возможно механическое повреждение лицевого нерва с формированием в дальнейшем пареза (ослабления) лицевого нерва. При тяжёлых родах возможно формирование ротационного подвывиха шейных позвонков.
Классификация и стадии развития перинатальной энцефалопатии
Перинатальные поражения ЦНС в зависимости от основного повреждающего фактора:
Длительность острого периода:
Восстановительный период длится от месяца до года, у недоношенных детей этот период удлиняется до 2 лет.
Осложнения перинатальной энцефалопатии
В случае тяжёлого поражения нервной системы и несвоевременного начала комплексного лечения впоследствии возможно формирование серьёзных нарушений:
Диагностика перинатальной энцефалопатии
В тех случаях, когда неврологические нарушения были ярко выражены изначально, диагноз перинатальной энцефалопатии устанавливается непосредственно в роддоме и ребёнок своевременно направляется в отделение неонатологии для интенсивной терапии.
В таком случае диагноз ставится на основании:
Далее невролог назначает ребёнку обследование:
При осмотре глазного дна отмечается ангиопатия сосудов глазного дна: сужение артерий, расширение и патологическая извитость вен. Однако провести осмотр глазного дна у маленького ребёнка не всегда удаётся, так как он не может зафиксировать взор в нужную для осмотра точку.
Лечение перинатальной энцефалопатии
Лечение перинатальной патологии в острый период проводится в отделении неонатологии.
Оперативное лечение может понадобиться при наличии у ребёнка большой гематомы внутри полости черепа — её удаление возможно только хирургическим путём.
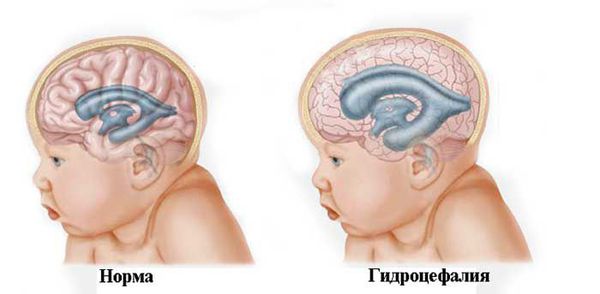
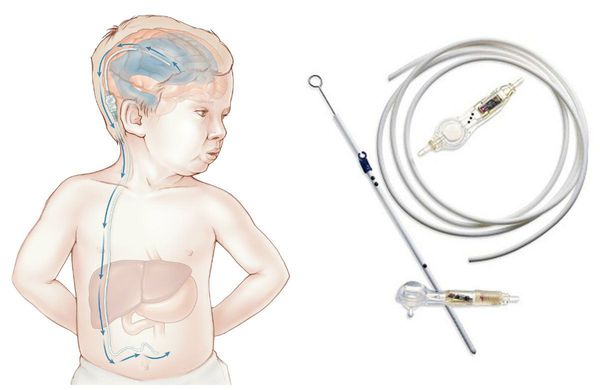
При нарастающей закрытой гидроцефалии, чтобы избежать атрофии головного мозга от сдавления его жидкостью, детям проводят шунтирующую операцию — устанавливают шунт (пластиковую трубочку, по которой лишняя жидкость из полости черепа отводится в брюшную полость и там всасывается).
Однако большинство родителей сталкивается с необходимостью лечения ребёнка с перинатальной энцефалопатией в восстановительный период до 1 года в связи с нарушением мышечного тонуса, задержкой развития, гипертензионно-гидроцефальным синдромом и прочими проявлениями.
Наибольшего эффекта можно добиться с помощью комплексного лечебного подхода.
ЛФК — лечебная физкультура. Может включать различные виды:
Микротоковая рефлексотерапия (МТРТ) — новая медицинская технология, разрешённая Минздравом РФ и рекомендованная для лечения детей с органическим поражением головного мозга, с задержками развития двигательного, речевого, психического развития и ДЦП. Лечение проводится в амбулаторном режиме в реабилитационных центрах в различных регионах РФ.
Лечебное воздействие физиологичное и безболезненное, оказывается токами микроамперного диапазона на нейрорефлекторные зоны на различных участках кожного покрова. Микротоки в 10 раз меньшие, чем при стандартной физиотерапии. Лечение проводится по индивидуальной схеме с учётом всех имеющихся у ребёнка проявлений перинатальной энцефалопатии.
В процессе лечения восстанавливается нормальная рефлекторная деятельность головного мозга, нормализуется мышечный тонус: спастичные (напряжённые) мышцы — расслабляются, гипотоничные (ослабленные) — стимулируются. МТРТ стабилизирует тонус сосудов головного мозга, что позволяет скомпенсировать внутричерепное давление.
Мочегонные препараты целесообразно использовать только при повышении внутричерепного давления (расширение ликворных пространств на НСГ, наличие клинических проявлений гипертензионно-гидроцефального синдрома).
Прогноз. Профилактика
В качестве профилактики необходимо минимизировать факторы риска при беременности и родоразрешении. Важнейшей задачей является предупреждение внутриутробной гипоксии. Для этого важно провести адекватную терапию имеющихся хронических заболеваний и своевременную коррекцию течения осложнённой беременности.