наследственная тромбофилия код мкб
Первичная тромбофилия
Рубрика МКБ-10: D68.5
Содержание
Определение и общие сведения [ править ]
Наследственная тромбофилия из-за врожденного дефицита белка S
Врожденный дефицит белка S является наследственным нарушением свертывания крови, характеризуется повторяющимися венозными тромбозами в связи со снижением уровня синтеза и/или активности белка S.
Распространенность частичного дефицита белка S (гетерозиготные особи) оценивается в 0.16-0.21% в общей популяции. Распространенность полного дефицита белка S (гомозиготные или компаундные гетерозиготные особи) неизвестна, но, вероятно, сопоставима с острым дефицитом белка С, которая оценивается на уровне 1 / 500,000. Мужчины и женщины в равной степени подвержены заболеванию.
Этиология и патогенез [ править ]
Дефицит белка S вызывается мутациями гена PROS1 (3К11-q11.2).
Клинические проявления [ править ]
При тяжелом дефиците белка S, болезнь проявляется в течение от нескольких часов до дней после рождения развитием молниеносной пурпуры или массивного венозного тромбоза. Молниеносная пурпура является опасным для жизни состоянием выраженной повышенной свертываемости во всем организме и вызывает некроз тканей. Тяжелая ретинопатия недоношенных также может развиваться у пациентов. Гетерозиготные пациенты, как правило, бессимптомны до взрослой жизни. Эпизоды тромбозов в основном вызываются действием факторов риска, такими как хирургическое вмешательство, беременность или длительная иммобилизация. Тромбоз глубоких вен нижних конечностей с или без легочной эмболии является наиболее распространенным проявлением заболевания. Артериальный тромбоз также может наблюдаться.
Первичная тромбофилия: Диагностика [ править ]
Диагноз основан на измерении уровней антигеннов белка S (содержание общего белка S или свободного белка S) и его антикоагулянтной активности. Существуют три биологические формы дефицита: тип I и тип III являются количественными дефицитами с низким содержанием уровня свободного антигена (нормальный уровень общего количества протеина S при типе III и сниженном уровне общего белка S при I типа дефицита). Тип II представляет собой качественный дефицит с нормальными уровнями общего и свободного белка S. Молекулярное тестирование доступно, но не является необходимым для постановки диагноза.
Дородовая диагностика возможна с помощью идентификации причинной мутации ДНК, полученной с помощью анализа ворсин хориона.
Дифференциальный диагноз [ править ]
Дифференциальный диагноз включает другие наследственные тромбофилии включая дефицит антитромбина и протеина С.
Первичная тромбофилия: Лечение [ править ]
Введение свежезамороженной плазмы может потребоваться для лечения неонатальной молниеносной пурпуры. Хирургическое вмешательство может потребоваться для удаления тромботических поражений. У пациентов с тромбозом используют антикоагулянты (гепарин, варфарин). Следует обратить внимание на риск кумарин-индуцированного некроза кожи. Профилактическое лечение в течение перипартального или периоперационного периодов показано в случаях семейной истории тяжелых тромботических заболеваний.
Прогноз неблагоприятный у гомозиготных или компаундных гетерозиготных пациентов. Прогноз благоприятный для гетерозиготных пациентов. При адекватной терапии и мониторинге, риск тромбоэмболических заболеваний заметно снижается. Смертность может быть результатом эмболии легочной артерии.
Профилактика [ править ]
Прочее [ править ]
Дефицит антитромбина ІІІ
Определение и общие сведения
Этиология и патогенез
Дефицит антитромбина III наследуется аутосомно-доминантно. Большинство носителей этой патологии гетерозиготы, гомозиготы погибают очень рано от тромбоэмболических осложнений.
В настоящее время описано до 80 мутаций гена, расположенного на длинном плече хромосомы 1. Частота этой патологии сильно отличается у разных этнических групп.
Различают два типа наследственного дефицита антитромбина III:
— тромбозы глубоких вен ног, илеофеморальные тромбозы (артериальные тромбозы не характерны для этой патологии);
— привычное невынашивание беременности;
— антенатальная гибель плода;
— тромбофилические осложнения после приема пероральных контрацептивов.
Функциональную активность антитромбина III определяют по способности образца плазмы ингибировать известное количество тромбина или фактора Ха, добавленного к образцу в присутствии или отсутствии гепарина.
При низкой активности антитромбина III основные тесты коагуляции не изменены, тесты на фибринолиз и время кровотечения нормальные, агрегация тромбоцитов в пределах нормы. При гепаринотерапии нет характерного адекватного увеличения АЧТВ (активированное частичное тромбиновое время).
В норме уровень антитромбина III составляет 85-110%. При беременности он несколько снижен и составляет 75-100%. Нижняя граница концентрации антитромбина III изменчива, поэтому необходимо учитывать не только уровень, но и клиническую ситуацию. Однако при снижении уровня антитромбина III ниже 30% пациентки погибают от тромбозов.
Основу лечения дефицита антитромбина III составляют противотромботические средства. При наличии симптомов тромбофилии лечение абсолютно необходимо. Для этих целей используют свежезамороженную плазму (как источник антитромбина III), низкомолекулярные гепарины (эноксапарин натрия, надропарин кальция, далтепарин натрия).
При низком уровне антитромбина III гепарин натрия не применяют, так как возможны гепаринорезистентность и гепарин-индуцированные тромбозы.
Вне беременности пациенткам может быть рекомендован длительный прием антагонистов витамина К (варфарин).
Другие нарушения свертываемости (D68)
Дефицит фактора VIII с сосудистым нарушением
Дефицит предшественника тромбопластина плазмы
Кровотечение во время длительного использования антикоагулянтов
При необходимости идентифицировать использованный антикоагулянт используют дополнительный код внешних причин (класс XX).
Исключены: длительное использование антикоагулянтов без кровотечения (Z92.1)
Исключена: недостаточность витамина K у новорожденного (P53)
Cопротивления к активированному протеину C [мутация фактора V Лейден]
Мутация гена протромбина
Наличие волчаночного антикоагулянта
Алфавитные указатели МКБ-10
Внешние причины травм — термины в этом разделе представляют собой не медицинские диагнозы, а описание обстоятельств, при которых произошло событие (Класс XX. Внешние причины заболеваемости и смертности. Коды рубрик V01-Y98).
Лекарственные средства и химические вещества — таблица лекарственных средств и химических веществ, вызвавших отравление или другие неблагоприятные реакции.
В России Международная классификация болезней 10-го пересмотра (МКБ-10) принята как единый нормативный документ для учета заболеваемости, причин обращений населения в медицинские учреждения всех ведомств, причин смерти.
МКБ-10 внедрена в практику здравоохранения на всей территории РФ в 1999 году приказом Минздрава России от 27.05.97 г. №170
Выход в свет нового пересмотра (МКБ-11) планируется ВОЗ в 2022 году.
Сокращения и условные обозначения в Международой классификации болезней 10-го пересмотра
БДУ — без дополнительных уточнений.
НКДР — не классифицированный(ая)(ое) в других рубриках.
† — код основной болезни. Главный код в системе двойного кодирования, содержит информацию основной генерализованной болезни.
* — факультативный код. Дополнительный код в системе двойного кодирования, содержит информацию о проявлении основной генерализованной болезни в отдельном органе или области тела.
Наследственная тромбофилия код мкб
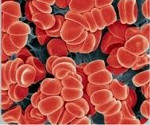
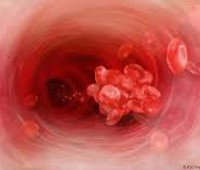
Тромбофилия – это наследственно обусловленная или приобретенная предрасположенность к формированию тромбов (кровяных сгустков) в просвете кровеносных сосудов. Тромбофилия не является заболеванием как таковым, а представляет собой состояние, которое в сочетании с факторами риска увеличивает вероятность возникновения тромбов в несколько раз.
Проявления тромбофилии связаны с образованием тромбов в венах и/или артериях, которые нарушают работу внутренних органов и представляют серьезную опасность для здоровья и жизни пациента. Однако многие люди с тромбофилией не испытывают в течение жизни никаких негативных последствий этого состояния.
Специфическое лечение тромбофилии отсутствует. Вопрос необходимости использования профилактической терапии, направленной на предотвращение формирования тромбов, решается индивидуально для каждого пациента. При высоком риске тромбоза профилактическое лечение позволяет предотвратить ряд тяжелых осложнений.
Прогноз тромбофилии зависит от ее типа, наличия и тяжести предшествующих случаев тромбоза, сопутствующих заболеваний.
Первичная тромбофилия, наследственная тромбофилия, врождённая тромбофилия, вторичная тромбофилия, приобретенная тромбофилия.
Hypercoagulability, coagulability, hypercoagulable state, hereditary thrombophilia, familial thrombophilia, primary thrombophilia, acquired thrombophilia, secondary thrombophilia.
Тромбофилия – это наследственно обусловленная или приобретенная предрасположенность к формированию тромбов (кровяных сгустков) в просвете кровеносных сосудов. Тромбофилия не является заболеванием как таковым, а представляет собой состояние, которое в сочетании с факторами риска увеличивает вероятность возникновения тромбов в несколько раз.
Проявления тромбофилии связаны с образованием тромбов в венах и/или артериях, которые нарушают работу внутренних органов и представляют серьезную опасность для здоровья и жизни пациента. Однако многие люди с тромбофилией не испытывают в течение жизни никаких негативных последствий этого состояния.
Специфическое лечение тромбофилии отсутствует. Вопрос необходимости использования профилактической терапии, направленной на предотвращение формирования тромбов, решается индивидуально для каждого пациента. При высоком риске тромбоза профилактическое лечение позволяет предотвратить ряд тяжелых осложнений.
Прогноз тромбофилии зависит от ее типа, наличия и тяжести предшествующих случаев тромбоза, сопутствующих заболеваний.
Большинство пациентов не знают о наличии у них тромбофилии до тех пор, пока не возникнет тромбоз или другие нарушения свертывания крови. Чаще всего при появлении тромба появляются следующие симптомы:
Общая информация о заболевании
Тромбофилия представляет собой состояние, при котором сгустки в крови образуются легче, чем в норме. Это происходит за счет изменения соотношения свертывающих и противосвертывающих факторов.
Нормальный процесс свертывания крови необходим для предотвращения кровотечений и заключается в формировании сгустков, которые закупоривают поврежденный сосуд. Процесс формирования сгустка происходит за счет взаимодействия ряда активных веществ – так называемых факторов свертывания. Существуют и противосвертывающие факторы, необходимые для предотвращения избыточного свертывания крови. При тромбофилии баланс этих веществ нарушен – либо повышается количество факторов свертывания, либо снижается количество противосвертывающих веществ. Это может привести к формированию тромбов – сгустков в просвете сосудов (вен или артерий), которые могут закупоривать просвет сосуда, нарушая таким образом кровоснабжение органов и тканей.
Тромбофилии делят на:
1. Врождённые (наследственные, первичные). Это тромбофилии, которые обусловлены наличием аномалий в генах, содержащих информацию о белках, участвующих в свертывании крови. Чаще всего встречается дефицит антитротромбина III, протеинов C и S, аномалия фактора V (мутация Лейден), аномалия протромбина G 202110А:
2. Приобретенные. К ним относятся тромбофилии, которые возникли в результате других заболеваний или приема лекарственных препаратов:
Тромбофилия может встречаться при заболеваниях, сопровождающихся повреждением сосудов, в частности при сахарном диабете, при котором, как известно, уровень инсулина снижен и, как следствие, повышена концентрация глюкозы в крови. Механизм повреждения сосудов при сахарном диабете до конца не выяснен, однако известно, что глюкоза токсически действует на клетки сосудов. Это приводит к выделению факторов свертывания, нарушению тока крови и избыточному тромбообразованию.
Чаще всего тромбофилия проявляется следующим образом.
Кто в группе риска?
Основой диагностики тромбофилий являются лабораторные исследования. Они должны проводиться через несколько недель после перенесенного эпизода тромбоза и вне приема препаратов, влияющих на свертывание крови.
Лечение тромбофилии зависит от степени риска тромбоза. Если он велик и превышает риск развития осложнений от терапии тромбофилии, то врач может назначить:
Специфической профилактики самой тромбофилии нет, однако большое значение имеет предупреждение тромбоза у пациентов с уже диагностированной тромбофилией: контроль за массой тела, рациональное питание, достаточное употребление жидкости (без кофеина, т. к. он сужает сосуды), умеренность в употреблении алкоголя, подвижный образ жизни, отказ от курения, ношение компрессионного белья при варикозе.
Рекомендуемые анализы
Тромбофилия
Тромбофилия – это предрасположенность к развитию рецидивирующих сосудистых тромбозов (преимущественно венозных) различной локализации. Заболевание обусловлено генетической или приобретенной патологией клеток крови или дефектами свертывающей системы крови. Клинически тромбофилия проявляется множественными тромбозами самой разной локализации. Повторяющиеся тромбозыв анамнезе пациента должны навести врача на мысль о наличие тромбофилии, что может быть подтверждено исследованиями крови и системы свертывания. Лечение тромбофилии зависит от ее вида. Как правило, применяются тромболитики, антикоагулянты и дезагреганты.
МКБ-10
Общие сведения
Тромбофилия – заболевание системы крови, проявляющееся в нарушении гемостаза и склонности к тромбообразованию. Проявлениями тромбофилии служат множественные и рецидивирующие тромбозы различной локализации, часто возникающие после физического перенапряжения, хирургического вмешательства, травмы, в связи с беременностью. Последствиями тромбофилии служат тромбозы глубоких вен, инфаркт миокарда, почки, инсульт, тромбоэмболия легочной артерии, нередко приводящие к летальному исходу.
Тромбофилия – широко распространенная патология. По утверждению некоторых авторов, теми или иными формами тромбофилии страдает около 40% взрослого населения. Отмечается постоянный рост количества тромбозов, обусловленный целым рядом факторов: «старением» населения, гиподинамией, наличием хронических заболеваний и т.д.
При образовании тромба нарушается нормальный кровоток, что может приводить к развитию опасных осложнений. Тромбоз сосудов мозга может стать причиной ишемического инсульта, тромбоз коронарных сосудов обуславливает развитие инфаркта миокарда, при тромбозе основных артерий конечностей возникает угроза омертвения тканей, приводящая к ампутации.
Тромбоз вен и артерий брыжейки кишечника (мезентериальных сосудов) вызывает некроз кишечника и развитие перитонита вследствие перфорации омертвевшего участка кишки. Микротромбозы сосудов плаценты могут привести к нарушению питания плодного яйца и самопроизвольному аборту.
При тромбозе глубоких вен нижних конечностей возникает опасность закупорки легочной артерии оторвавшимся тромбом (тромбоэмболия легочной артерии), а в отдаленном периоде увеличивается риск развития хронической венозной недостаточности. По данным международной статистики, количество тромбозов глубоких вен нижних конечностей постоянно растет. В настоящее время частота обращения по поводу флеботромбозов составляет 150 случаев на 100 тыс. человек в год.
Причины
Риск развития тромбофилии увеличивается при наличии генетической предрасположенности (наследственные тромбофилии), некоторых приобретенных заболеваниях крови (тромбоцитозы, этитремия, антифосфолипидный синдром), атеросклерозе, злокачественных новообразованиях, мерцательной аритмии, варикозном расширении вен нижних конечностей, ряде аутоиммунных заболеваний, артериальной гипертензии.
Вероятность развития тромбофилии возрастает после перенесенного инсульта или инфаркта. Риск образования тромбов увеличивается после травм и хирургических вмешательств, при продолжительной малоподвижности, при ожирении, в период беременности, при приеме гормональных контрацептивов. Фактором риска является курение. Тромбофилия чаще развивается у пациентов старших возрастных групп.
Классификация
Можно выделить две основные группы тромбофилий.
1. Тромбофилии, обусловленные нарушением клеточного состава и реологических свойств крови. К развитию этой группы тромбофилий приводят следующие состояния:
2. Тромбофилии, возникающие вследствие первичных нарушений гемостаза. К этой группе относятся состояния, обусловленные избытком или недостатком факторов свертывания.
Все виды нарушений состава крови и дефекты свертывающей системы крови могут быть как врожденными, так и приобретенными.
Симптомы тромбофилии
Клинические проявления тромбофилии при образовании конкретного тромба зависят от места поражения, степени нарушения кровообращения и наличия сопутствующей (фоновой) патологии. О тромбофилии свидетельствуют множественные тромбозы различной локализации, инфаркты органов, развивающиеся у относительно молодых пациентов, тромбоэмболии в бассейне легочной артерии.
Диагностика
Диагноз тромбофилии выставляется на основании склонности к рецидивирующему образованию тромбов различной локализации, семейной истории (наследственная предрасположенность), характерных результатах лабораторных анализов. Пациенты с венозными тромбозами, как правило, обращаются за помощью к флебологу. Наличие повторных тромбозов в анамнезе позволяет врачу заподозрить тромбофилию и назначить проведение соответствующих лабораторных исследований. Лабораторные тесты проводятся в два этапа. Вначале определяются наиболее распространенные виды и группы тромбофилий, затем выполняются подтверждающие узкоспециализированные исследования.
Лечение тромбофилии
При лечении тромбофилии зачастую необходимо одновременно решать две задачи: принимать меры по борьбе с тромбозами и проводить терапию основного заболевания, которое привело к рецидивирующему образованию тромбов. Лечение тромбозов заключается в назначении тромболитиков и антикоагулянтов.
При тромбофилиях, обусловленных нарушением клеточного состава и реологических свойств крови пациентам назначают дезагреганты и антикоагулянты (дипиридамол, ацетилсалициловая кислота). Применяется гирудотерапия (лечение пиявками) различные методики гемодилюциии (тромбоцитоферез, эритроцитоферез).
В терапии тромбофилии, обусловленной дефицитом антикоагулянтов и факторов свертывания, используются струйные переливания больших количество свежей или свежезамороженной плазмы. При некоторых болезнях, способствующих развитию тромбофилии (болезнь Мошкович, тромбоцитопеническая пурпура) для спасения жизни больных требуется быстрое заменное переливание крови (массивный плазмаферез в сочетании со струйным введением свежезамороженной плазмы).
Профилактика
Своевременное предупреждение и лечение тромбофилии становится возможным при раннем выявлении лиц с предрасположенностью к образованию тромбов. Необходимо устранять факторы, способствующие развитию заболевания (длительное охлаждение, ожирение, чрезмерные физические нагрузки, гипокинезия). Не следует принимать гормональные противозачаточные средства и проводить внутривенные манипуляции без назначения врача.
Генетический риск развития тромбофилии (расширенный)
Комплексный генетический анализ, который позволяет определить риск тромбофилии. Он представляет собой молекулярно-генетическое исследование генов факторов свертываемости крови, тромбоцитарных рецепторов, фибринолиза, обмена фолиевой кислоты, изменение активности которых напрямую или опосредованно обуславливает склонность к повышенному тромбообразованию.
Какой биоматериал можно использовать для исследования?
Буккальный (щечный) эпителий, венозную кровь.
Как правильно подготовиться к исследованию?
Подготовки не требуется.
Подробнее об исследовании
В результате различных патологических процессов в сосудах могут образоваться тромбы, которые блокируют кровоток. Это самое частое и неблагоприятное проявление наследственной тромбофилии – повышенной склонности к тромбообразованию, связанной с определенными генетическими дефектами. Она может приводить к развитию артериальных и венозных тромбозов, которые в свою очередь зачастую являются причиной инфаркта миокарда, ишемической болезни сердца, инсульта, тромбоэмболии легочной артерии и др.
В систему гемостаза входят факторы свертывающей и противосвертывающей систем крови. В нормальном состоянии они находятся в равновесии и обеспечивают физиологические свойства крови, не допуская повышенного тромбообразования или, наоборот, кровоточивости. Но при воздействии внешних или внутренних факторов это равновесие может нарушаться.
В развитии наследственной тромбофилии, как правило, принимают участие гены факторов свертывания крови и фибринолиза, а также гены ферментов, контролирующих обмен фолиевой кислоты. Нарушения в этом обмене могут привести к тромботическим и атеросклеротическим поражениям сосудов (через повышение уровня гомоцистеина в крови).
Наиболее значимым нарушением, ведущим к тромбофилии, является мутация в гене фактора свертываемости 5 (F5), ее еще называют Лейденской. Она проявляется устойчивостью фактора 5 к активированному протеину С и увеличением скорости образования тромбина, в результате чего и происходит усиление процессов свертываемости крови. Также важную роль в развитии тромбофилии играет мутация в гене протромбина (F2), связанная с повышением уровня синтеза данного фактора свертываемости. При наличии этих мутаций риск тромбозов значительно возрастает, особенно за счет провоцирующих факторов: приема оральных контрацептивов, избыточного веса, гиподинамии и т. д.
У носительниц таких мутаций высока вероятность неблагоприятного течения беременности, например невынашивания беременности, задержки внутриутробного развития плода.
Предрасположенность к тромбозам может быть также обусловлена мутацией гена FGB, кодирующего бета-субъединицу фибриногена (генетический маркер FGB (-455GA). Результатом является повышение синтеза фибриногена, вследствие чего возрастает риск периферического и коронарного тромбоза, риск тромбоэмболических осложнений во время беременности, при родах и в послеродовом периоде.
Среди факторов, повышающих риск развития тромбоза, очень важны гены тромбоцитарных рецепторов. В данном исследовании проводится анализ генетического маркера гена тромбоцитарного рецептора к коллагену (ITGA2 807 C>T) и фибриногену (ITGB3 1565T>C). При дефекте гена рецептора к коллагену усиливается прилипание тромбоцитов к эндотелию сосудов и к друг к другу, что ведет к повышенному тромбообразованию. При анализе генетического маркера ITGB3 1565T>C возможно выявить эффективность или неэффективность антиагрегантной терапии аспирином. При нарушениях, обусловленных мутациями в этих генах, повышается риск тромбозов, инфаркта миокарда, ишемического инсульта.
С тромбофилией могут быть связаны не только нарушения свертывающей системы крови, но и мутации генов фибринолитической системы. Генетический маркер SERPINE1 (-675 5G>4G) – ингибитор активатора плазминогена – основного компонента антисвертывающей системы крови. Неблагоприятный вариант этого маркера приводит к ослаблению фибринолитической активности крови и, как следствие, повышает риск сосудистых осложнений, различных тромбоэмболий. Мутация гена SERPINE1 также отмечается при некоторых осложнениях беременности (невынашивание беременности, задержка развития плода).
Кроме мутаций факторов свертывающей и противосвертывающей систем, как значимую причину тромбофилии рассматривают повышенный уровень гомоцистеина. При чрезмерном накоплении он оказывает токсическое действие на эндотелий сосудов, поражает сосудистую стенку. В месте повреждения образуются тромбы, там же может осесть избыточный холестерин. Эти процессы приводят к закупориванию сосудов. Избыточное содержание гомоцистеина (гипергомоцистеинемия) увеличивает вероятность развития тромбозов в кровеносных сосудах (как в артериях, так и в венах). Одной из причин повышения уровня гомоцистеина является снижение активности ферментов, обеспечивающих его обмен (в исследование включен ген MTHFR). Помимо генетического риска развития гипергомоцистеинемии и ассоциированных с ней заболеваний, наличие изменений в данном гене позволяет определить предрасположенность и к неблагоприятному течению беременности (фетоплацентарной недостаточности, незаращению нервной трубки и другим осложнениям для плода). При изменениях в фолатном цикле в качестве профилактики назначаются фолиевая кислота и витамины В6, В12. Продолжительность терапии и дозировка препаратов может определяться на основании генотипа, уровня гомоцистеина и особенностей сопутствующих факторов риска у пациента.
Заподозрить наследственную предрасположенность к тромбофилии возможно при семейной и/или личной истории тромботических заболеваний (тромбоз глубоких вен, варикозная болезнь и др.) и также в акушерской практике – при тромбоэмболических осложнениях у женщин во время беременности, в послеродовом периоде.
Комплексное молекулярно-генетическое исследование позволяет оценить генетический риск тробофилии. Зная о генетической предрасположенности можно предотвратить своевременными профилактическими мероприятиями развитие сердечно-сосудистых нарушений..
Факторы риска развития тромбофилии:
Когда назначается исследование?
Что означают результаты?
По результатам комплексного исследования 10 значимых генетических маркеров выдается заключение врача-генетика, которое позволит оценить риск тромбофилии, спрогнозировать развитие таких заболеваний как тромбоз, тромбоэмболия, инфаркт, или вероятность осложнений, связанных с нарушением гемостаза, при беременности, выбрать направления оптимальной профилактики, а при уже имеющихся клинических проявлениях детально разобраться в их причинах.
Генетические маркеры
Литература