14-16 октября, Алматы, «Атакент»
150 участников из 10 стран. Новинки рынка стоматологии. Цены от производителей
Общая информация
Краткое описание
Коды по МКБ 10:
Q 68.3 Врожденное искривление бедра
Q 68.4 Врожденное искривление костей голени
М 21.0 Приобретенная вальгусная деформация конечности
М 21.1 Приобретенная варусная деформация конечности
М 21.9 Приобретенная деформация конечности неуточненная
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
1. Вальгусная деформация.
2. Варусная деформация.
3. Антекурвационная деформация.
4. Рекурвационная деформация.
Диагностика
Диагностические критерии
Жалобы и анамнез: в анамнезе при врожденной патологии в возрасте 1-1,5 лет выявляется деформация конечности, появляется прихрамывание, позднее боли в суставах после длительной ходьбы. При приобретенной патологии деформация конечности появляется после снятия гипсовой иммобилизации или в ближайшее время после нагрузки.
Физикальное обследование: нарушение походки (хромота или прихрамывание), выраженная осевая деформация конечности, ограничение движений в близлежащем суставе.
Лабораторные исследования: изменений в клинических, биохимических анализах при отсутствии сопутствующей патологии не наблюдается.
Инструментальные исследования: на рентгенограммах костей в двух проекциях отмечается осевая деформация костей.
Минимум обследования при направлении в стационар:
3. Анализ на ВИЧ, гепатиты в случае перенесенных ранее оперативных вмешательств.
Основные диагностические мероприятия:
1. Общий анализ крови (6 параметров), гематокрит, тромбоциты, свертываемость.
2. Определение остаточного азота, мочевины, общего белка, билирубина, кальция, калия, натрия, глюкозы, АЛТ, АСТ.
3. Определение группы крови и резус-фактора.
4. Общий анализ мочи.
5. Рентгенография тазобедренных суставов в прямой проекции и с внутренней ротацией.
6. УЗИ органов брюшной полости.
9. ИФА на маркеры гепатитов В, С, Д, ВИЧ по показаниям.
10. ЭМГ по показаниям.
Дополнительные диагностические мероприятия:
1. Анализ мочи по Аддису-Каковскому по показаниям.
2. Анализ мочи по Зимницкому по показаниям.
3. Посев мочи с отбором колоний по показаниям.
4. Рентгенография грудной клетки по показаниям.
5. ЭхоКГ по показаниям.
Дифференциальный диагноз
Признак
Деформация конечностей
Фиброзная дисплазия
Незавершенный остеогенез
Начало появления деформации
В раннем детстве или после травмы
Постепенное проявление деформации
Варусные, вальгусные, рекурвационные, антекурвационные
Сложные осевые и комбинированные
Сложные осевые и комбинированные
Структура кости не изменена
Истончение кортикального слоя, наличие очагов
Атрофия диафизов, прозрачность костной ткани
Лечение
Тактика лечения
Цели лечения: устранение осевой деформации конечности, статической боли в суставах путем корригирующих остеотомий с наложением аппаратов ЧКО или металло-остеосинтезом.
Медикаментозное лечение:
3. Обезболивающая терапия в послеоперационном периоде с первых суток (трамадол, кетонал, триган, промедол) по показаниям, в течение 3-5 суток.
5. С целью профилактики гипокальциемии (глюконат кальция, кальций-Дз Никомед, кальцид, остеогенон) перорально с 7-10 суток после операции, в возрастной дозировке.
Переливание компонентов крови (СЗП, эрмасса одногруппная) интраоперационно и в послеоперационном периоде по показаниям.
Профилактические мероприятия: профилактика бактериальной и вирусной инфекции.
1. Профилактика контрактур и тугоподвижности сустава.
2. Профилактика остеопороза.
Основные медикаменты:
5. Препараты кальция в таблетках
Дополнительные медикаменты:
1. Препараты железа перорально
2. Растворы глюкозы в\в
3. Раствор NaCl 0,9% в\в
5. Металлоконструкции и аппараты ЧКО
Индикаторы эффективности лечения:
1. Устранение осевой деформации конечности.
2. Восстановление полного объема движений в суставах.
Госпитализация
Показания к госпитализации: плановое, выраженная осевая деформация костей верхних и нижних конечностей с нарушением функции конечности в виде хромоты, ограничения функции сустава, боли в близлежащих суставах.
Поражение надколенника (педиатрия)
14-16 октября, Алматы, «Атакент»
150 участников из 10 стран. Новинки рынка стоматологии. Цены от производителей
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
• определение резус фактора; • контрольная рентгенография коленного сустава в 2-х проекциях.
• крепитация в коленных суставах, чувство неустойчивости в коленном суставе, периодическую припухлость, слабость и судороги в мышцах голени и бедра[3].
Анамнез:
• наличие в анамнезе травмы (или нескольких травм) коленного сустава, приводившие к вывиху надколенника.
Дифференциальный диагноз
2-х стороний полиартрит.
2-х стороний полиартрит
Лечение
ванкомицин: 15 мг/кг/сут., не более 2 г/сут. в 4 введения, внутривенно, каждая доза должна вводиться не менее 60 мин.
10-14 лет: разовая доза 0,3-0,5 мл (3-5 мг), суточная – 1-1,5 мл (10-15 мг).
Медикаментозное лечение оказываемое на амбулаторном уровне: не проводится.
Медикаментозное лечение, оказываемое на стационарном уровне
Перечень основных лекарственных средств (имеющих 100% вероятности проведения):
Другие виды лечения, оказываемые на этапе скорой неотложной помощи: не проводится.
Хирургическое вмешательство оказываемое в амбулаторных условиях: не проводится.
Хирургическое вмешательство оказываемое в стационарных условиях
• профилактика миграции металлоконструкций (точное выполнение методики операций, использование качественных, зарегистрированных в Республике Казахстан металлоконструкций и инструментов).
Рекомендации по навыкам здорового образа жизни: плавание, закаливание, занятие спортом плавание [2].
Журнал «Боль. Суставы. Позвоночник» 1 (05) 2012
Вернуться к номеру
К вопросу о синдроме гипермобильности суставов
Версия для печати
Резюме. В статье приведены диагностические критерии синдрома гипермобильности суставов, рассмотрены осложнения этого синдрома, описаны терапевтические мероприятия.
Резюме. У статті наведені діагностичні критерії синдрому гіпермобільності суглобів, розглянуті ускладнення цього синдрому, описані терапевтичні заходи.
Summary. The article deals with diagnostic criteria of joint hypermobility syndrome; complications of this syndrome were considered, therapeutic measures were described.
Ключевые слова: синдром гипермобильности суставов, критерии, лечение.
Ключові слова: синдром гіпермобільності суглобів, критерії, лікування.
Key words: joint hypermobility syndrome, criteria, treatment.
Актуальность
На протяжении многих лет проблема гипермобильного синдрома как проявления дисплазии соединительной ткани сохраняет свою актуальность ввиду значительной его распространенности (от 10 до 21,5 % в общей популяции [1]). Среди европейских школьников синдром гипермобильности суставов (СГС) диагностирован в 11,7 % случаев [2]. Наши эпидемиологические исследования распространенности СГС среди 10–17-летних школьников Украины и Беларуси позволили получить похожие цифры — 11,2–12,8 %. Значимость проблемы гипермобильного синдрома заключается в том, что он играет важную роль в развитии ребенка и во многом определяет характер и течение ряда заболеваний опорно-двигательного аппарата, сердечно-сосудистой системы, нарушений вегетативного статуса, нередко ведет к хронизации основной патологии, в связи с чем рассматривается как серьезный инвалидизирующий фактор и является одной из причин резистентности к терапии.
Несмотря на важность проблемы, диагностика СГС врачами первичного звена остается очень низкой. Так, еще в 1997 г. Н.И. Коршунов, В.Р. Гауэрт указали на то, что процент выявления СГС на уровне поликлиник составляет 0 [3]. Через 15 лет ситуация практически не изменилась. Настоящей статьей мы начинаем дискуссию по проблеме СГС на страницах нашего журнала.
Определение, терминология
Само понятие «гипермобильность суставов» (ГС) определяется как состояние, при котором большинство суставов имеет диапазон движений больший, чем обычный для данного возраста, пола и национальности [4]. Гиперподвижность может быть наследственной, приобретаться со временем в результате тренировок или развиваться в результате хронических заболеваний (при миопатиях, эндокринных расстройствах, родовой травме позвоночника и др.) [5].
Термин «синдром гипермобильности суставов» впервые предложен группой исследователей J. Kirk, B. Ansell, Е. Bywaters в 1967 г. [6]. Они описывали состояние, при котором имеются определенные жалобы со стороны опорно-двигательного аппарата у гипермобильных лиц при отсутствии признаков какого-либо другого ревматического заболевания
Позже R. Grahame [5] вывел формулу СГС:
СГС = ГС + симптоматика.
Диагностика
На сегодняшний день существует ряд нормативных документов, в которых описаны алгоритмы диагностики и лечения заболеваний, связанных с нарушением соединительной ткани, а именно:
— Берлинская нозология наследственных нарушений соединительной ткани [7];
— международные рекомендации по диагностике синдрома Марфана — Гентские критерии [8];
— международные рекомендации по диагностике синдрома Элерса — Данло — Вилльфраншские критерии [9];
— международные рекомендации по диагностике синдрома гипермобильности суставов — Брайтонские критерии (1998) с последующей их ревизией R. Grahamе [5];
— наследственные нарушения соединительной ткани. Российские рекомендации [10].
Согласно этим документам, для диагностики ГС следует использовать критерии P. Beighton (1998) [9]:
— пассивное сгибание метакарпального сустава V пальца на 90° в обе стороны (1–2 балла, рис. 1А);
— пассивное сгибание I пальца в сторону предплечья при сгибании в лучезапястном суставе (1–2 балла, рис. 1Б);
— переразгибание обоих локтевых суставов > 10 градусов (1–2 балла, рис. 1В);
— переразгибание обоих коленных суставов > 10 градусов (1–2 балла, рис. 1Г);
— при наклоне вперед при фиксированных коленных суставах плоскости ладоней пациента касаются пола (1 балл).
Отсутствие гипермобильности определяют при сумме баллов от 1 до 4, умеренную ГС — от 5 до 6 баллов, выраженную ГС — от 7 до 9 баллов.
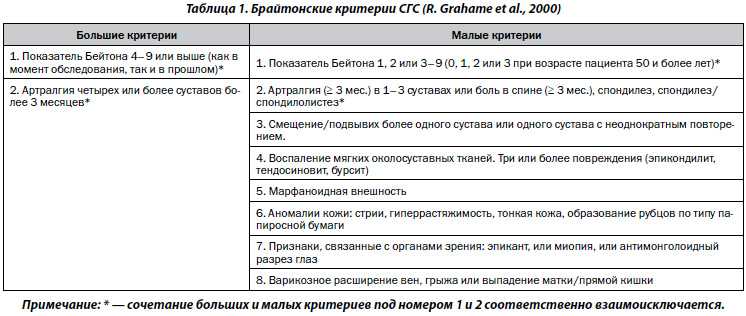
Для постановки диагноза СГС следует пользоваться Брайтонскими критериями СГС [5], которые разделены на большие и малые (табл. 1).
СГС диагностируют при наличии двух больших критериев, либо одного большого и двух малых критериев, либо четырех малых критериев. Два малых критерия достаточны, если имеется близкий родственник, страдающий данным заболеванием. СГС исключают при наличии синдромов Марфана или Элерса — Данло. Полагают, что диагноз СГС у части пациентов сегодня может быть подтвержден лабораторными исследованиями уровня гликопротеина тенасцина Х сыворотки крови (антигена мышечных сухожилий) и при анализе полиморфизма гена тенасцина Х.
Диагноз МКБ. В МКБ-10 СГС имеет свой шифр и отнесен к классу XIII — болезни костно-мышечной системы и соединительной ткани, к блоку М30-М36 — системные поражения соединительной ткани и имеет код M35.7 — гипермобильный синдром (Hypermobility syndrome). В МКБ-10 представлены и синонимы ГМС — семейная слабость связочного аппарата (Familial ligamentous laxity) и доброкачественная гипермобильность суставов (Benign joint hypermobility).
Проблемы диагностики. Несмотря на существующие диагностические критерии, предложенный подход к диагнозу не однозначен. Поскольку СГС сопровождается поражением не только суставов, а также принимая во внимание генетические аспекты и результаты ряда морфологических исследований волокнистых структур соединительной ткани, некоторые ученые [6] предлагали СГС и синдромы Элерса — Данло и Марфана относить к одной группе наследственных болезней, расположенных на противоположных концах клинического спектра. Сегодня термины «синдром гипермобильности суставов» и «гипермобильный тип синдрома Элерса — Данло» пытаются рассматривать как синонимы [5], но проведенный в 2009 году анализ 3330 публикаций [11] не выявил надежных дифференциальных критериев для СГС, семейной ГС и гипермобильного типа синдрома Элерса — Данло. Авторы считают причиной СГС у детей генетические особенности и предлагают мультидисциплинарный подход к ведению детей с ГС и артралгией с целью раннего начала профилактических мероприятий. Кроме того, для описания комбинации гипермобильности суставов и функциональных признаков предлагается предпочтительно употреблять термин «синдром гипермобильности суставов», поскольку понятие «доброкачественная» в описании «синдрома доброкачественной гипермобильности суставов» вводит в заблуждение и является нецелесообразным.
Сложности диагностики СГС у детей и подростков заключаются еще и в том, что Брайтонские критерии создавались для лиц от 16 до 85 лет и их применение в детской практике, возможно, неоправданно. Так, проведенные эпидемиологические исследования среди 6022 14-летних детей Великобритании [12] выявили 4 и более баллов по шкале Бейтон у 27,5 % девочек и 10,6 % мальчиков. По мнению авторов, полученные результаты поставили под сомнение существующие диагностические критерии ГС в отношении молодых пациентов, опорно-двигательный аппарат которых находится в состоянии роста и развития, что требует уточнения диагностических алгоритмов СГС у детей и подростков.
Осложнения СГС
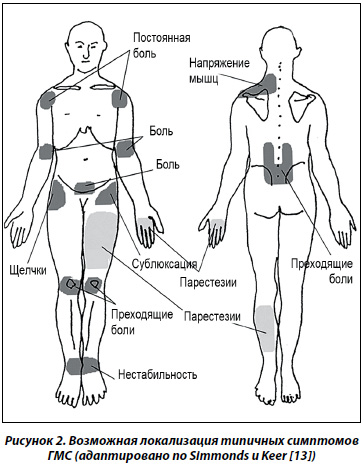
В клинике СГС, кроме перечисленных выше симптомов, выделяют хронический болевой синдром с локализацией в типичных местах [13] (рис. 2). Такие пациенты жалуются на постоянные боли в плечевых и локтевых суставах, преходящие боли в коленных суставах и в поясничном отделе позвоночника, нестабильность голеностопных и тазобедренных суставов, щелчки и подвывихи суставов, парестезии в бедренных, икроножных мышцах и дистальных фалангах кистей, миофасциальные боли в мышцах плечевого пояса.
Мы предлагаем адаптированную по R. Keer, R. Grahame (2003)[4] с дополнениями классификацию нервно-мышечных и скелетно-мышечных осложнений и клинических проявлений, которые наблюдаются у детей с синдромом гипермобильности суставов.
1. Острые или травматические:
– рецидивирующие повреждения голеностопного сустава;
– коленного сустава, разрыв мениска;
– острые и рецидивирующие вывихи/подвывихи:
Метаболические нарушения у детей с синдромом гипермобильности суставов
Боли в суставах встречаются у детей достаточно часто, особенно в младшем возрасте, при этом причины артралгий весьма разнообразны. Одна из них — гипермобильность суставов (ГС), которая чаще всего является следствием соединит
Боли в суставах встречаются у детей достаточно часто, особенно в младшем возрасте, при этом причины артралгий весьма разнообразны. Одна из них — гипермобильность суставов (ГС), которая чаще всего является следствием соединительнотканной дисплазии. Синдром гипермобильности суставов (СГС) — это состояние, при котором у детей или взрослых людей с ГС имеются определенные жалобы со стороны опорно-двигательного аппарата, но при этом нет признаков какого-либо ревматического заболевания. Несмотря на то, что ГС в популяции встречается с частотой 10–15%, лишь небольшая часть этих пациентов предъявляет жалобы на боли в суставах. В своей работе мы попытались найти причины, способствующие появлению артралгий у детей с ГС. Для этого был проведен сравнительный анализ клинических проявлений в двух группах пациентов с выраженными признаками дисплазии соединительной ткани (ДСТ), отличающихся друг от друга наличием либо отсутствием артралгий.
Для выявления метаболических нарушений у большей части обследованных детей определяли содержание микроэлементов в волосах. Известно, что микроэлементный статус характеризует минеральный обмен в организме. При этом наиболее актуальным для детей является состояние обмена кальция, фосфора, магния, железа, меди, серы, кобальта, селена, цинка, марганца, фтора, ванадия, кремния и бора, так как эти микроэлементы участвуют не только в процессе роста и развития ребенка, но и принимают активное участие в метаболизме коллагена.
С целью диагностики нарушений обмена соединительной ткани на биохимическом уровне было проведено исследование показателей синтеза и распада костного коллагена. Анализировались содержание остеокальцина, дезоксипиридинолина, показатели бета-Сross laps и TPINP-тесты в сыворотке крови и уровень пирилинкса D в суточной моче.
Повышенная подвижность суставов может быть обусловлена не только слабостью связочного аппарата, но и снижением мышечного тонуса. В последнее время появилось много сообщений о наличии у больных ДСТ вторичной карнитиновой недостаточности [2]. В связи с этим следующей задачей исследования явилось определение содержания карнитина в крови у детей, страдающих рецидивирующими болями в суставах на фоне ГС.
Карнитин — биологически активное вещество, родственное витаминам группы В, которое играет важную роль в клеточном метаболизме и, прежде всего, в энергетическом обмене. Он является переносчиком жирных кислот через мембраны клеток из цитоплазмы в митохондрии, где эти кислоты окисляются (процесс бета-окисления) с образованием большого количества метаболической энергии (в форме АТФ). Карнитин участвует в связывании и выведении из тканей органических кислот, которые, являясь промежуточными продуктами окислительных процессов, способны тормозить активность ряда ферментов и негативно воздействовать на мембранные структуры.
Вторичная недостаточность карнитина может быть вызвана различными причинами. Например, низким содержанием аминокислот или кофакторов синтеза карнитина, недостаточным поступлением их с пищей, снижением реабсорбции в желудочно-кишечном тракте либо почках, а также быстрым потреблением, например, у спортсменов при чрезмерной мышечной нагрузке. При недостаточности карнитина органами-мишенями в первую очередь становятся скелетные мышцы и миокард, а во вторую — клетки головного мозга и другие органы. Основными клиническими проявлениями дефицита карнитина являются: сниженная работоспособность, мышечная слабость, сонливость, нарушение функционального состояния сердечно-сосудистой системы и печени.
Клиническая характеристика детей и методы исследования
Обследовано 106 детей (мальчиков — 64, девочек — 42) в возрасте от 3 до 18 лет с признаками ДСТ. Все дети были разделены на две группы: 1-я группа — дети с артралгиями — 47 человек, 2-я группа — (группа сравнения) состояла из 59 детей с выраженными признаками ДСТ, но не имеющих артралгий. Клиническое обследование включало оценку физического развития, выявление фенотипических, клинико-инструментальных и лабораторных признаков ДСТ. Степень тяжести ДСТ определяли балльным методом [3]. Для исключения воспалительного характера суставных жалоб у детей 1-й группы проводилось полное артрологическое обследование — клинический и биохимический анализ крови, определение ревматоидного и антинуклеарного факторов, антител к хламидиям, бактериям кишечной группы (псевдотуберкулез, сальмонеллез). Дополнительно анализировались результаты реакции Манту, мазки из зева и носа на микробный пейзаж и вирусы. Все дети были осмотрены окулистом с помощью щелевой лампы.
При наличии хронических очагов инфекции больные консультировались ЛОР-врачом, стоматологом. Проводилось рентгенологическое или УЗИ-исследование суставов. Уровень общего карнитина в крови определяли энзиматическим методом с использованием коммерческих наборов. Исследование микроэлементного состава волос проводили в лаборатории Центра биохимических исследований (г. Санкт-Петербург) методом атомно-абсорбционной спектроскопии (спектрометр Karl Zeiss AAS-30). Косвенный показатель распада коллагена 1-го типа (бета-Сross laps тест) и интенсивность костеобразования (остеокальцин, общий аминотерминальный пропептид коллагена 1-го типа, TPINP) определяли с помощью тест-системы Elecsys. Костная денситометрия поясничного отдела позвоночника проводилась методом двухэнергетической рентгеновской абсорбциометрии DXA (L2-L4) с помощью остеоденситометра, оснащенного «детской» программой. Полученные данные обработаны с помощью статистических методов (c2, критерий Стьюдента) с помощью статистического пакета SPSS 16.
Результаты и обсуждение
Умеренная степень тяжести ДСТ диагностирована у 25 из 106 обследованных детей, у остальных (81 чел.) — выраженная. С помощью статистических методов исследования установлено, что у детей с артралгиями достоверно чаще встречались изменения со стороны кожи (нежная, гиперэластичная), тонкая (выражен венозный рисунок), геморрагический синдром (склонность к носовым кровотечениям, повышенная «синячковость»), выраженная гипермобильность и подвывихи суставов, плоскостопие, синдром «прямой спины», склонность к образованию «натоптышей» или гигром и hallux valgus. В анамнезе этих детей достоверно чаще имелись указания на дисплазию тазобедренных суставов, склонность к частым вирусным и бактериальным инфекциям. При осмотре пациентов данной группы с большей частотой, чем у лиц контрольной группы (табл. 1), выявлялась асимметрия длины нижних конечностей, хруст в суставах, астенический тип конституции, плохая переносимость физической нагрузки. У детей с артралгиями достоверно чаще диагностировались дискинезия желчевыводящих путей, психические и поведенческие (астенические, аффективные, панические) расстройства.
Результаты исследования представлены в табл. 1.
Представленные данные наглядно демонстрируют, что у детей с гипермобильным синдромом выражены и другие признаки соединительнотканной дисплазии, что необходимо учитывать в дифференциальной диагностике причин ГС. Кроме этого у них достоверно чаще встречались признаки, характеризующие тканевую ранимость, склонность к геморрагиям. Это может объяснять тот факт, что у большей части детей боли в суставах были связаны с физической нагрузкой или травмой. Нередко предпосылкой к появлению артралгий являлось перерастяжение связочного аппарата суставов, например, при выполнении упражнений «мост», «шпагат».
У детей раннего возраста боли в суставах, как правило, провоцировались длительной ходьбой в неудобной или неразношенной обуви, особенно в случаях плосковальгусной деформации стопы. Малышам свойственно острое начало заболевания, которое проявляется внезапной хромотой и практическим отсутствием (в связи с возрастом) жалоб на боли в суставах. У подростков с ГС причиной артралгий чаще всего являлась реакция со стороны околосуставных мягких тканей, которая возникала в результате микротравматизации сухожилий и связок даже при незначительных физических нагрузках с последующим развитием легких воспалительных явлений. У ряда обследованных артралгии возникли на фоне изменения метеорологических условий или гормонального статуса.
По нашим наблюдениям, артралгии у детей нередко имитировали боли в костях и нередко сочетались с выраженной остеопенией. В этой ситуации проведение денситометрии являлось решающим в дифференциальной диагностике болевого синдрома. В нашем исследовании частота встречаемости снижения костной массы по результатам денситометрии была примерно одинаковой в обеих группах. В группе детей с артралгиями было обследовано 28 детей, у 17 было выявлено снижение костной массы (60,7%), в группе без артралгий обследовано 19 детей, снижение показателей зафиксировано у 12 человек (63,15%).
У ряда детей происходила соматизация конфликтов в семье, школе, что было характерно и для маленьких детей. Так, например, если в семье появлялся второй ребенок, то для привлечения к себе внимания дети жаловались на боли в ногах. Почти у половины пациентов с артралгиями выявлено наличие очагов хронической инфекции.
Основными проявлениями синдрома ГС у детей являлись жалобы на боли в суставах (чаще коленных, несколько реже тазобедренных, голеностопных и др.), хромота, нарушение функции суставов, плохая переносимость физической нагрузки, невозможность преодолевать большие расстояния.
У одной группы детей суставные боли возникали чаще к вечеру. По характеру они были достаточно интенсивными и иногда приводили к кратковременной контрактуре сустава. У другой группы наших пациентов жалобы на боли в суставах были непостоянны, обычно после физического переутомления, в послеобеденные часы, ночью или реже — утром. Боль не имела сковывающего характера и, несмотря на выраженную интенсивность, объем движений в суставах чаще всего был полностью сохранен.
У всех пациентов с болями в суставах отсутствовали другие признаки воспаления, такие как припухлость сустава, повышение местной температуры и т. д.
У 4 из 47 (8,5%) детей с артралгиями была выявлена асимметрия длины нижних конечностей, которая приводила к статическим нарушениям и, как следствие, к локальной дисплазии тазобедренного сустава, что всегда сопровождалось разной степени выраженности сколиозом. Практически у всех (85,1%) диагностировано плоскостопие, которое является одной из значимых причин болевого синдрома. Поэтому большое место в лечении артралгий уделяется коррекции плоскостопия.
Рентгенологическое обследование суставов у детей данной группы не выявило какой-либо патологии. Однако при УЗ-исследовании суставов у 11 детей отмечены дистрофические изменения со стороны хрящевых структур. Показатели лабораторного обследования свидетельствовали об отсутствии воспалительного процесса.
По результатам лабораторного обследования показателей синтеза и распада коллагена у детей обеих групп с ДСТ у большинства были выявлены признаки повышенного синтеза и распада костного коллагена. Однако достоверные различия в показателях метаболизма коллагена в группах детей с ДСТ, отличающихся между собой наличием или отсутствием артралгий, отсутствуют.
В табл. 2 представлены результаты исследования содержания микроэлементов в волосах в сопоставлении с их безопасно допустимыми уровнями (БДУ) у детей.
Результаты исследования показали, что более половины обследованных детей с ДСТ имеют разной степени выраженности дефицит макро- и микроэлементов (магния, кальция, железа, цинка, кремния, марганца, меди, селена), принимающих участие в синтезе, созревании коллагеновых волокон, протеогликанов, минерализации костной ткани, а также стабилизации клеточных мембран многочисленных компонентов соединительной ткани. Достоверных различий по содержанию макро- и микроэлементов в группах больных ДСТ в зависимости от наличия или отсутствия артралгии нами не получено.
У 20 детей с жалобами на боли в суставах был определен уровень карнитина в сыворотке крови (табл. 3).
Результаты исследования свидетельствуют о достоверном снижении (по сравнению с группой детей, не имевших признаков ДСТ) содержания общего карнитина у детей с СГС, что подтверждает наличие у них вторичной митохондриальной недостаточности.
Таким образом, проведенные исследования выявили у детей с гипермобильным синдромом достоверное снижение уровня большинства макро- и микроэлементов, общего карнитина в сыворотке крови, нарушение показателей синтеза и распада коллагена, что требует проведения соответствующей метаболитной коррекции.
С целью коррекции недостаточности микроэлементов могут быть использованы препараты микроэлементов. Для стимуляции обмена коллагена при отсутствии оксалатно-кальциевой кристаллоурии — витамин С, магниевая соль оротовой кислоты в сочетании с пиаскледином, хондропротекторами и аминокислотами (L-лизин, L-пролин).
При недостаточности карнитина необходимо использовать препарат Элькар 20% (L-карнитин). Исследования, проведенные в Педиатрической медицинской академии (г. Санкт-Петербург), показали высокую эффективность и безопасность препарата Элькар. Детям Элькар назначают в дозе 30–50 мг/кг веса в сутки в 2 приема. Курс лечения — 1 месяц.
Литература
Т. И. Кадурина*, доктор медицинских наук, профессор
Л. Н. Аббакумова**, кандидат медицинских наук, доцент
*МАПО, **СПбГПМА, Санкт-Петербург