Нейробластома
Нейробластома – эмбриональная опухоль, возникающая в процессе внутриутробного или раннего постнатального периода жизни из стволовых нервных клеток – нейробластов.
Впервые описание этой опухоли, названной впоследствии «детской глиомой», дал Рудольф Людвиг Карл Вирхов в 1864 году. Позднее в 1891 году немецким ученым патоморфологом Феликсом Маршандом был определен источник опухоли – клетки симпатической нервной системы и надпочечники. Симпатическая нервная система – это часть автономной (вегетативной) нервной системы. Она контролирует непроизвольную работу внутренних органов человека, например, работу сердца, кишечника, мочевого пузыря, процесс кровообращения.
Эпидемиология
Нейробластома составляет около 7-8% от всех злокачественных новообразований в детском и подростковом возрасте. Это наиболее часто возникающий вид детских новообразований после опухолей кроветворной и центральной нервной системы. Примерно 40% случаев заболевания встречается на первом году жизни, с возрастом количество случаев уменьшается. Средний возраст на момент диагностирования составляет 19 месяцев.
Причины и риски
Причины появления опухоли до конца не изучены. Нейробластома возникает в том случае, когда нормальные нейробласты не созревают в нервные клетки. Вместо этого они продолжают бесконтрольно расти и делиться. Предполагают, что эти несозревшие (эмбриональные) нервные клетки начинают мутировать еще до рождения ребенка, когда начинают меняться хромосомы и/или происходит сбой в регулировании работы генов. Как подтверждают актуальные исследования, у большинства детей болезнь не является наследственной̆. Только около 1% случаев нейробластомы имеют наследственную основу, чаще всего, вследствие мутаций в гене, который̆ называется ALK (или ген киназы анапластической лимфомы), либо в гене PHOX2B. На сегодняшний̆ день нет клинических исследований, доказывающих, что внешние факторы (окружающая среда, вредные условия работы родителей ребенка, прием каких-либо медикаментов, курение и употребление алкоголя во время беременности) могут стать причиной болезни.
Клиническая картина при нейробластоме
Нейробластома может возникать в любой анатомической области, где располагается симпатическая нервная система: надпочечники, шейный, грудной и брюшной симпатический отделы, параганглии.
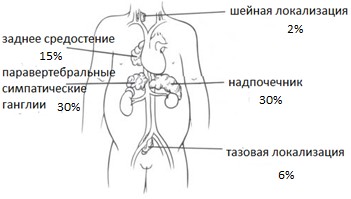
Самой частой локализацией нейробластомы является забрюшинное пространство (одинаково часто опухоль диагностируется в надпочечниках и паравертебральных забрюшинных ганглиях). У 15% детей нейробластома локализуется в заднем средостении. Реже опухоль возникает в области таза (6%) и шеи (2%) (рис. 1).
Рис. 1. Локализация нейробластомы
При ранних стадиях заболевания у многих детей может не быть никаких симптомов. Опухоль у них находят случайно, например, при плановом УЗИ обследовании младенцев при диспансеризации. Как правило, жалобы у детей появляются тогда, когда опухоль уже успела сильно вырасти и давит на соседние органы, нарушая их работу, или когда опухоль дала метастазы.
Среди общих симптомов заболевания можно выделить следующие: потеря веса, слабость, костные и суставные боли, некупируемая диарея.
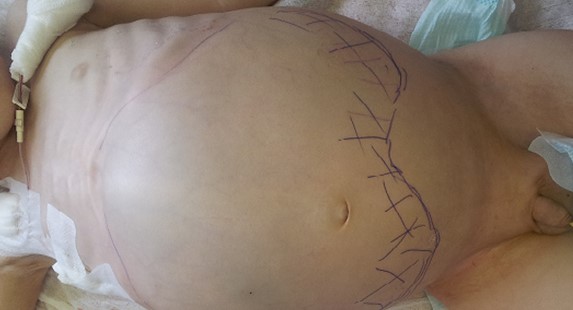
Большинство проявлений болезни и их выраженность зависят от расположения опухоли и ее взаимосвязи с соседними органами и тканями. Так, для пациентов в возрасте до 2-х лет при забрюшинной локализации характерно увеличение размеров живота, лихорадка и потеря веса. Нейробластома забрюшинного пространства пальпируется через переднюю брюшную стенку в виде бугристого, несмещаемого опухолевого узла (рис. 2). У детей старшего возраста заболевание может манифестировать болевым синдромом, обусловленным метастатическим поражением костей, респираторными нарушениями, увеличением размеров живота, появлением запоров. У пациентов с большими забрюшинными опухолями можно обнаружить развитую сеть подкожных вен, развернутые края грудной клетки.
Рис. 2. Нейробластома забрюшинного пространства
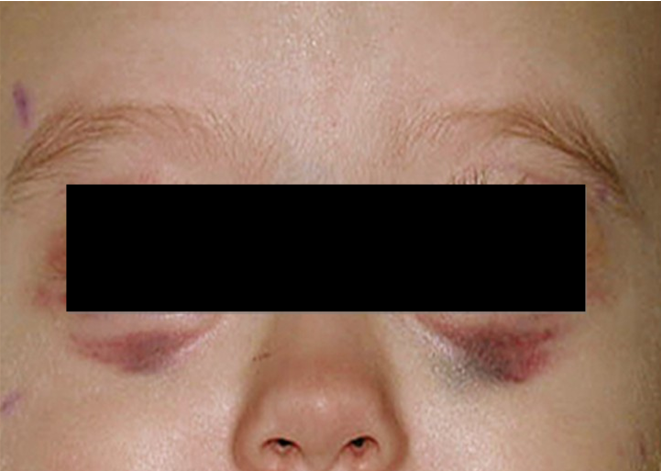
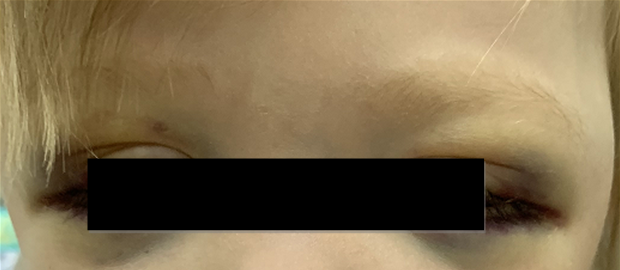
Локализация опухоли в шейно-грудном отделе симпатического отдела позвоночника вызывает синдром Горнера (сужение зрачка, разные размеры зрачков, покраснение и/или опущение верхнего века и небольшое поднятие нижнего). Другими изменениями в области глаз могут быть кровоизлияния в кожу или слизистую оболочку, «синяки» на веках и под глазами. На поздней стадии болезни иногда появляются черные круги вокруг глаз (гематома в виде очков) (рис. 3).
Рис. 3.1. Симптом «очков»
Рис. 3.2. Симптом «очков» при метастазах в орбиту
Поражение заднего средостения может стать причиной сухого кашля, дыхательных расстройств, деформации грудной клетки, частого срыгивания. При локализации опухоли в полости таза отмечают нарушение функции тазовых органов (периодическое недержание мочи, нарушение акта дефекации), отёки нижних конечностей.
При распространении опухоли в позвоночный канал и сдавлении ею спинного мозга могут развиваться слабость в ногах, неустойивость походки, параличи нижних конечностей, а также дисфункции органов малого таза (задержка мочеиспускания или непроизвольное мочеиспускание, запоры).
Редко, примерно в 2-4% всех случаев, у детей встречается ассоциированный с нейробластомой церебеллярный синдром («опсоклонус-миоклонус» или энцефалопатия Кинсбурна), характеризующийся некоординированными, нерегулярными движениями туловища и конечностей, миоклонусом и хаотичными движениями глазных яблок.
Нейробластома ‒ гормонопродуцирующая опухоль, способная к секреции физиологически активных веществ – катехоламинов ‒ адреналина, норадреналина и дофамина. В моче, как правило, повышено выведение их метаболитов ‒ ванилилминдальной и гомованилиновой кислот. В 95% случаев гормональная активность нейробластомы тем больше, чем выше степень её злокачественности. Эффекты секретируемых гормонов вызывают специфические клинические симптомы нейробластомы ‒ резкое повышение артериального давления, диарею (вызывается секрецией вазоактивного интестинального полипептида), потливость, эмоциональную лабильность, периодическое повышение температуры.
Нейробластома метастазирует чаще всего в костный мозг, кости, в отдаленные лимфатические узлы, печень или кожу, редко — в головной мозг или легкие. Признаки отдалённых метастазов можно обнаружить в виде экзофтальма, кровоизлияний в орбиты, опухолевых узлов на голове.
Среди особенностей течения нейробластомы можно выделить следующие:
Гистологическая классификация
Существующая гистологическая классификация нейробластомы INPC-Shimada основана на степени зрелости (дифференцировки) опухолевой ткани и выделяет 4 категории (от недифференцированных до зрелых форм):
1) нейробластома, бедная шванновской стромой: недифференцированная, низкодифференцированная, дифференцированная;
2) нодулярная ганглионейробластома;
Стадии заболевания
Существует несколько систем стадирования нейробластомы. Наиболее точной является модифицированная система, разработанная Международным противораковым союзом (INSS) (табл. 1).
Диагностика нейробластомы
Лабораторные методы
В клиническом анализе крови при поражении костного мозга может наблюдаться снижение показателей крови: анемия, лейконейтропения, тромбоцитопения.
В сыворотке крови также можно определить специфические для нейробластомы маркеры: нейрон-специфическую енолазу (НСЕ), уровень метаболитов катехоламинов, лактатдегидрогеназу (ЛДГ) и ферритин.
Простым в выполнении специализированным тестом при диагностировании нейробластомы является определение уровня ванилилминдальной и гомованилиновой кислот в анализе мочи. Их также называют «тестом на оценку метаболитов катехоламинов в моче». Данный анализ может проводиться при сборе мочи ребенка в течение суток или в однократной порции мочи.
Перед началом специфической терапии всегда проводится верификация диагноза; диагноз нейробластомы ставится при гистологическом исследовании биоптата первичной опухоли или метастазов, или при сочетании наличия опухолевых клеток в костном мозге и повышенного уровня суточной экскреции катехоламинов.
Молекулярно-генетическое исследование
Инструментальные методы
Ультразвуковое исследование
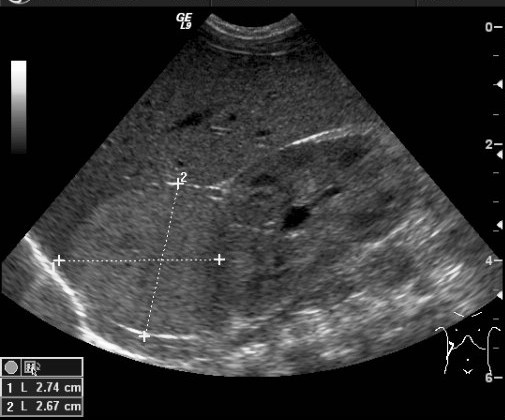
Ультразвуковой метод исследования позволяет выявить наличие опухоли и ее расположение по отношению к внутренним органам. УЗИ позволяет оценить степень местного и отдаленного распространения злокачественного процесса и выявляет метастатическое поражение печени и лимфатических узлов (рис. 4).
Рис. 4. УЗИ образования правого надпочечника
Компьютерная томография брюшной полости и забрюшинного пространства
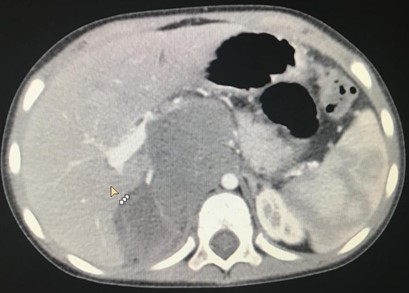
Компьютерная томография более детально дает информацию об анатомическом отношении опухоли к окружающим тканям и органам, позволяет оценить структуру опухоли (рис. 5).
Рис. 5. КТ нейрогенного образования забрюшинного пространства справа
Магнитно-резонансная томография органов брюшной полости, забрюшинного пространства и позвоночника
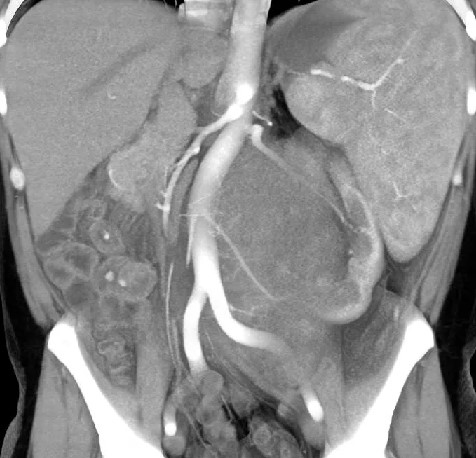
МРТ органов брюшной полости и забрюшинного пространства ‒ это безопасный и высокоинформативный метод исследования, который позволяет не только уточнить локализацию опухоли, точные размеры новообразования и соотношение его с окружающими тканями, но и выявить метастатические очаги в печени и брюшной полости. Также МРТ дает возможность оценить состояние костных структур и мягких тканей позвоночного столба и позвоночного канала (рис. 6).
Рис. 6. МРТ нейрогенного образования забрюшинного пространства слева
Радиоизотопные исследования
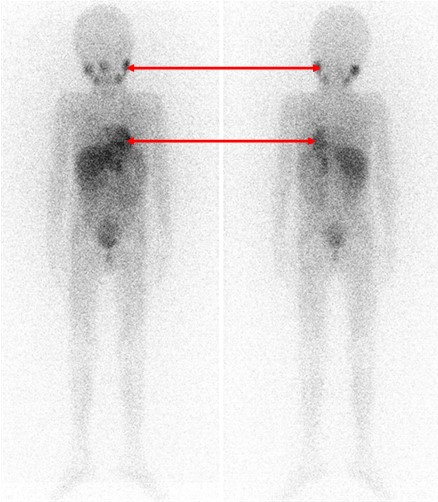
Одним из наиболее информативных специфических методов топической диагностики нейробластом является сцинтиграфия с метайодбензилгуанидином (МЙБГ), меченным 123I. МЙБГ по своей химической структуре сходен с катехоламинами в организме. Это вещество концентрируется в тех опухолях, которые вырабатывают катехоламины. МЙБГ метят радиоактивным изотопом йода (например, 123I) в безопасной для жизни дозе, и готовый препарат внутривенно вводят в кровоток. Накапливаясь в клетках опухоли, он дает излучение. Эти сигналы регистрирует специальная камера и переводит их в изображение. Таким образом, метод позволяет выявить не только первичную опухоль, но и наличие регионарных и отдаленных метастазов (рис. 7).
Рис. 7. Сцинтиграфия с метайодбензилгуанидином (визуализируется первичная паравертебральная опухоль с метастазами в кости черепа)
Остеосцинтиграфия – метод сканирования костей скелета с помощью внутривенного введения радиофармпрепарата. Радиофармпрепарат накапливается участками, пораженными опухолевыми клетками в костях, что видно на снимках, выполняемых гамма-камерой. Таким образом, данный метод исследования позволяет выявить возможные метастазы костей скелета.
Исследование костного мозга (миелограмма и трепанобиопсия) используется для уточнения наличия поражения опухолевыми клетками костного мозга.
Лечение нейробластомы
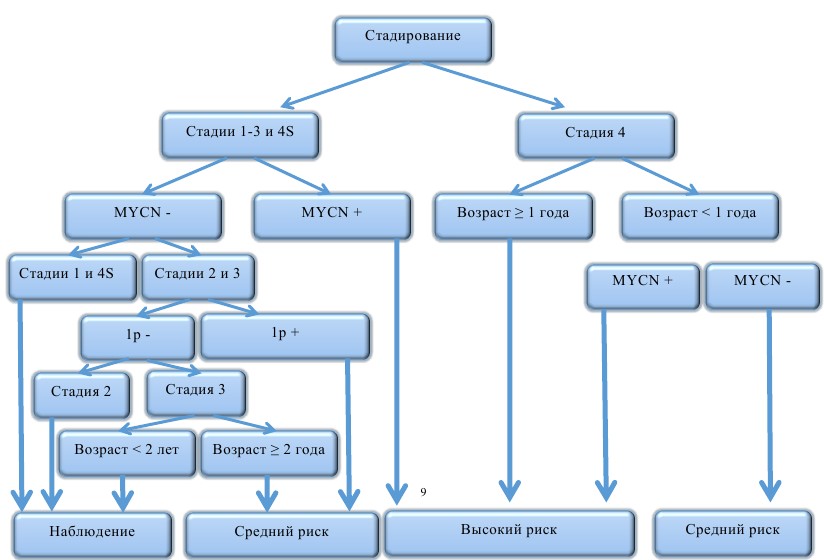
Учитывая разнообразные сценарии развития исхода заболевания (от спонтанной регрессии до летального исхода от прогрессирования), в терапии нейробластомы предлагаются риск-адаптированные принципы. Стратификация пациентов проводится согласно факторам риска до начала лечения (как правило, это клинические и молекулярно-генетические данные) и на основании ответа опухоли во время лечения (response-adapted). При выделении групп риска перед началом лечения используются следующие прогностические критерии: стадия заболевания, возраст на момент диагностики, результаты молекулярно-генетических данных — амплификация MYCN и делеция короткого плеча 1р (рис. 8).
Рис. 8. Стратификация пациентов на группы риска согласно наличию факторов неблагоприятного прогноза
Неоадъювантная (предоперационая) полихимиотерапия
Особенности хирургического лечения
Адъювантная (постоперационная) полихимиотерапия
Лекарственное лечение необходимо начать через 5-7 дней после оперативного вмешательства. При отсутствии показаний для проведения 2-й линии полихимиотерапии в схемах лечения используются те же базовые препараты, как и при неоадъювантной терапии.
Лучевая терапия
В случае наличия неблагоприятных прогностических факторов, в частности выявления в опухоли мутации MYCN онкогена, рекомендовано проведение высокодозной полихимиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток.
Для больных с высоким риском развития рецидива (распространенные стадии заболевания с наличием неблагоприятных молекулярно-генетических маркеров) рекомендовано проведение «поддерживающей» дифференцирующей терапии 13-цис-ретиноевой кислотой и пассивной иммунотерапией антиGD2 моноклональными антителами.
Иммунотерапия
Иммунотерапия – новый метод лечения нейробластомы, который используется для уничтожения раковых клеток. Дисиалоганглиозид GD2 – молекула- антиген, экспрессируемая клетками нейробластомы, это делает ее идеальной мишенью для иммунотерапии антителами: антитело действует против этой молекулы. Клетки иммунной системы могут способствовать гибели клеток нейробластомы.
В НМИЦ онкологии им. Н.Н. Петрова проводятся все этапы лечения, включая минимально-инвазивные операции (лапаро- и торакоскопические), тандемную трансплантацию и пассивную иммунотерапию.
Интенсифицируя терапию у детей с нейробластомой группы высокого риска (с включением тандемной высокодозной полихимиотерапии в консолидацию и пассивной иммунотерапии в постконсолидацию) удалось повысить результаты выживаемости на 20%.
Рекомендации после лечения
СПИСОК ЛИТЕРАТУРЫ
Авторы:
Под научной редакцией:
Кулева С.А.
Заведующий детским онкологическим отделением, врач-детский онколог, ведущий научный сотрудник, профессор, доктор медицинских наук, главный внештатный детский специалист-онколог Комитета по здравоохранению Санкт-Петербурга
Нейробластома у детей. Клинические рекомендации.
Нейробластома у детей
Оглавление
Ключевые слова
Список сокращений
д.м.н. – доктор медицинских наук
ДНК – дезоксирибонуклеиновая кислота
ЗНО – злокачественное новообразование
к.м.н. – кандидат медицинских наук
МЗ РФ – Министерство здравоохранения Российской Федерации
НИИ ДОГ – Научно-исследовательский институт детской онкологии и гематологии Федерального государственного бюджетного учреждения «Российский онкологический научный центр имени Н.Н.Блохина» Минздрава России
НСЕ – нейроспецифическая нейролаза
РКИ – рандомизированное контролируемое исследование
РФ – Российская Федерация
УЗВТ – ультразвуковая томография
INSS – International Neuroblastoma Staging System — международная система стадирования нейробластомы
1. Краткая информация
1.1 Определение
Нейробластома — эмбриональная опухоль симпатической нервной системы, возникающая в процессе внутриутробного или раннего постнатального периода жизни из нейробластов нервного гребня.
1.2 Этиология и патогенез
Нарушение дифференцировки нейробластов нервного гребня во внутриутробном периоде в следствии возникновения мутаций определенных локусов генов супрессоров опухолевого роста приводит к неконтролируемой пролиферации этих клеток — развитию злокачественной опухоли.
1.3 Эпидемиология
Нейрогенные опухоли являются одними из наиболее распространенных в детском возрасте и составляют 8 – 10% от всех опухолевых заболеваний, в возрастной группе до 5 лет — 80% [1]. Средний возраст на момент постановки диагноза составляет 22 месяца. Мальчики заболевают несколько чаще девочек, соотношение 1,2:1.
Как правило, нейрогенные опухоли поражают надпочечники (35%), симпатические ганглии забрюшинного пространства (30-35%), заднего средостения (20%), шеи (1-5%), малого таза (2-3%), реже опухоль может развиться в вилочковой железе, легких, почке и др.
Метастазирование протекает как лимфогенным, так и гематогенным путем: наиболее часто поражаются печень, легкие, кости и костный мозг.
Возраст пациента и стадия заболевания являются основными факторами, влияющими на прогноз заболевания. Клинические проявления весьма разнообразны и неспецифичны: астения, потливость, лихорадка, боли в области первичной опухоли или метастазов. Для пациентов в возрасте до 2-х лет характерно увеличение размеров живота, лихорадка и потеря веса. У детей старшего возраста заболевание может манифестировать болевым синдромом, обусловленным метастатическим поражением костей, респираторными нарушениями, увеличением размеров живота, абдоминальных болей, запоров.
Гистологически группа нейрогенных опухолей представлена широким спектром новообразований: ганглионевромой, недифференцированной нейробластомой и– ганглионейробластома (промежуточный вариант) [1, 4].
Ганглионевромы —доброкачественные, медленно растущие опухоли, которые как правило, локализуются в средостении, реже — в забрюшинном пространстве и малом тазу [3].
Ганглионейробластомы — опухоли с низкой дифференцировкой, состоящие из ганглиозной стромы и нейробластов различной степени дифференцировки, вплоть до зрелых ганглиозных клеток [2].
1.4. Кодирование по МКБ 10
C47.3 – ЗНО Периферических нервов грудной клетки
C47.4 – ЗНО Периферических нервов живота
C47.5 – ЗНО Периферических нервов таза
C47.6 – ЗНО Периферических нервов туловища неуточненное
C47.8 – ЗНО Поражение периферических нервов и вегетативной нервной системы, выходящее за пределы одной и более вышеуказанных локализаций
C47.9 – ЗНО Периферических нервов и вегетативной нервной системы неуточненной локализации
С48.0 – ЗНО Забрюшинного пространства
С74.0 – ЗНО Коры надпочечника
С74.1 – ЗНО Мозгового слоя надпочечника
С74.9 – ЗНО Надпочечника неуточненной части
С76.0 – ЗНО Головы, лица и шеи
С76.1 – ЗНО Грудной клетки
С76.7 – ЗНО Других неуточненных локализаций
С76.8 – ЗНО Других неточно обозначенных локализаций, выходящее за пределы одной и более вышеуказанных локализаций
1.5. Классификация нейробластомы
Классификация TNM (International Society of Paediatric Oncology, (SIOP), 1987)
Стадирование нейробластомы по системе International Neuroblastoma Staging System (Международной системы стадирования нейробластомы, INSS):
Классификация групп риска:
Наиболее распространено стадирование заболевания по критериям INSS, которые основаны на клинических, рентгенологических, хирургических и патоморфологических признаках в сочетании с возрастом, что определяет прогностические группы для определения программы специального лечения.
В последние несколько лет появились маркеры, определяющие биологическую характеристику и поведение нейробластомы, а также прогноз заболевания. Среди них: плоидность опухолевой клетки (ДНК индекс), число копий протоонкогена N-myc в геноме опухолевой клетки, и гистологические признаки Shimada [9].
Стадия по системе INSS
Возраст, лет
Амплификация N-myc
Гистология по Shimada
плоидность
Группа риска
2. Диагностика
2.1. Жалобы и анамнез
Комментарии: Нередко за несколько месяцев до обращения к врачу возникает общий опухолевый симптомокомплекс. В ходе сбора анамнеза рекомендовано обратить внимание на длительность того или иного клинического проявления, его динамику, изменение внешнего вида и поведения пациента. Локализация опухоли в шейно-грудном отделе симпатического ствола вызывает синдром Горнера на ранних стадиях заболевания, затруднения при дыхании и глотании. Поражение заднего средостения может стать причиной сухого кашля, дыхательных расстройств, деформации грудной клетки, частого срыгивания. При абдоминальной локализации характерны частые периодические боли в животе, понос и рвота без видимых причин, запоры, боль в конечностях. При локализации опухоли в полости таза отмечают нарушение функции тазовых органов, отёки нижних конечностей. Особое внимание следует уделить онкологическому семейному анамнезу, а также обратить внимание на возможность воздействия на родителей неблагоприятных факторов: профессиональных вредностей, облучения матери во время беременности и др. Необходимо помнить, что опухолевое поражение нередко сочетается с пороками развития.
2.2. Физикальное обследование
У пациентов с большими забрюшинными опухолями можно обнаружить развитую сеть подкожных вен, развернутые края грудной клетки. Признаки отдалённых метастазов можно обнаружить в виде экзофтальма, кровоизлияний в орбиты, опухолевых узлов на голове.
2.3 Лабораторные исследования
Комментарии: в анализах периферической крови у больных нейробластомой часто удается обнаружить ускоренную СОЭ, анемический синдром различной степени выраженности. Возможна как лейкопения, так и лейкоцитоз. Нередко отмечается сдвиг формулы влево, в основном за счет метамиелоцитов, в ряде случаев до миелоцитов. Довольно часто наблюдается тромбоцитоз. Анализы мочи в подавляющем большинстве случаев – без отклонений от нормы, изредка имеет место непостоянная микрогематурия и альбуминемия. В крови или моче больного определяются и другие опухолевые маркеры: НСЕ, ферритин и ганглиосайды.
2.3 Инструментальные исследования
Комментарии: УЗВТ является наиболее распространенным методом в диагностике объемных образований в проекции живота. КТ или МРТ применяются для определения распространенности опухолевого процесса. При этом МРТ позволяет точнее определить взаимосвязь опухоли и магистральных сосудов, а также позволяет выявить наличие интраспинального распространения. Преимущество КТ заключается в возможности определения кальцификатов, характерных для большинства больных с нейробластомой. Для установления метастатического поражения костей используется радиоактивный технеций. В последние годы для диагностики нейробластомы предложено проведение радиоизотопного исследования с применением метайодобензилгванидина (131- J – mJBG), аналога гуанетидина, меченного йодом-123. Сканирование, проведенное после введения этого препарата, позволяет выявить первичную остаточную и рецидивную опухоль, наличие метастатического поражения костного мозга, костей, лимфатических узлов и мягких тканей. Диагностическая ценность метода составляет более, чем 90%. Костно-мозговую пункцию или трепанобиопсию грудины, крыла подвздошной кости, пяточной кости или большеберцовой кости (не менее чем из 3 зон) относят к обязательным диагностическим процедурам. Полученные аспираты или биоптаты изучают цитологически, иммунологически или с помощью проточной цитометрии. Заключительный этап клинической диагностики заболевания — аспирационная или открытая биопсия опухоли с цитологическим, гистологическим, иммунологическим и молекулярно-генетическим исследованием полученного материала. Проведенный алгоритм обследования позволит установить группу риска пациентов и начать соответствующее лечение.
3. Лечение
3.1 Консервативное лечение
Препараты, мг/м 2 (мг/кг)
Схема 1, дни цикла
Схема 2, дни цикла
Карбоплатин 560** (18)
0, 1, 2, 42, 43, 44, 63,64, 65
Циклофосфамид** 1000 (33)
Курс
Препараты
Дни введения
Дозировка, мг/м? (мг/кг)
Способ введения
Комментарии: Для пациентов с нейробластомой IV стадии группы высокого риска показано проведение 5 курсов ПХТ, для пациентов с нейробластомой III стадии группы высокого риска показано проведение 4 курсов ПХТ.
3.2 Хирургическое лечение
Комментарии: Целью оперативного вмешательства при подозрении на нейробластому является гистологическая верификация диагноза, радикальное удаление первичной опухоли или максимального объема опухолевой ткани. Во время операции устанавливается вовлечение в опухолевый процесс лимфатических узлов, что необходимо для стадирования болезни. Кроме этого, опухолевая ткань направляется на биологическое исследование с целью установления группы риска.
Пациентам с интрадуральным поражением и парезами конечностей рекомендовано выполнение биопсии (следует избегать ламинэктомии) с целью морфологической верификации диагноза с последующим назначением ПХТ.
У пациентов с 4/4S стадиями болезни младше 2 месяцев при выполнении хирургического вмешательства велик риск развития осложнений, что обусловлено гепатомегалией, которая может сочетаться с коагулопатией. С целью предотвращения развития осложнений рекомендовано исследовать экстраабдоминальные участки поражения (подкожные узлы или лимфатические узлы), если они диагностированы. Для пациентов в возрасте до 1 года, у которых велик риск развития послеоперационных осложнений в виде расхождения краев раны, инфекции, геморрагического синдрома, целесообразно на первом этапе выполнить биопсию костного мозга с последующим гистологическим и биологическим исследованием.
3.3 Лучевая терапия
Коментарии: Остаточная активная опухоль определяется либо гистологическим исследованием, либо при радиоизотопном исследовании (РИД) с MIBG.
Пациентам группы среднего риска, имеющим симптомы, связанные с органной недостаточностью из-за остаточного объема опухоли и не реагирующие на ПХТ, а также пациентам с остаточной опухолью после хирургического лечения, проведенного по поводу местного рецидива, возникшего через 3 месяца после завершения программного лечения, может быть проведена ЛТ.
3.4 Лечение больных с нейробластомой группы высокого риска
Уровень убедительности С (уровень доказательности – 3)
Уровень убедительности С (уровень доказательности – 3)
3.5 Высокодозная химиотерапия с трансплантацией аутологичных стволовых клеток
Треосульфан 10000 мг/м 2 /сут. 4, 3, 2 дни (курсовая доза 30000 мг/м 2 )
Мелфалан** 80 мг/м 2 /сут. 3, 2 дни (курсовая доза 160 мг/м 2 )
Трансплантация ауто-ГСК – 0 день.
Коментарии: в день 0 ауто-ГСК размораживаются в водяной бане при температуре 38-40 0 и переливаются внутривенно. Гранулоцитарные колониестимулирующие факторы (Г-КСФ) назначаются после инфузии ауто-ГСК в день 0.
4. Реабилитация
5. Профилактика и диспансерное наблюдение
6. Дополнительная информация, влияющая на течение и исход заболевания
6.1 Оценка факторов риска при нейробластоме
Неблагоприятные факторы прогноза:
6.2 Критерии ответа на проводимое лечение
Выполнен осмотр врачом-детским онкологом перед началом каждого курса полихимиотерапии
Выполнен осмотр врачом – детским онкологом и врачом-радиологом перед каждым курсом лучевой терапии
Выполнено повторное ультразвуковое исследование зоны первичного опухолевого очага и органов брюшной полости и забрюшинного пространства (перед хирургическим вмешательством)
Выполнена повторная магнитно-резонансная томография с внутривенным контрастированием зоны первичного опухолевого очага и/или компьютерная томография зоны первичного опухолевого очага (перед хирургическим вмешательством)
Выполнен осмотр врачом – детским онкологом и врачом-радиологом перед каждым курсом лучевой терапии
Выполнена повторная компьютерная томография органов грудной клетки не реже 1 раза в 2 месяца
Выполнен общий (клинический) анализ крови развернутый с подсчетом лейкоцитарной формулы перед началом каждого курса полихимиотерапии и не реже 1 раза в неделю при проведении полихимиотерапии
Выполнен анализ крови биохимический общетерапевтический (мочевина, креатинин, общий белок, альбумин, общий билирубин, аланинаминотрансфераза, аспартатаминотрансфераза, лактатдегидрогеназа, натрий, калий, хлор) перед началом каждого курса полихимиотерапии и не реже 1 раза в неделю при проведении полихимиотерапии
Выполнен анализ мочи общий перед началом каждого курса полихимиотерапии и не реже 1 раза в неделю при проведении полихимиотерапии
Выполнено назначение антибактериальных лекарственных препаратов (при фебрильной нейтропении)
Отсутствие гнойно-септических осложнений
Список литературы
Приложение А1. Состав рабочей группы
Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Таблица П1 – Уровни доказательств в соответствии с международными критериями
Категория
Доказательства
Мета-анализ рандомизированных контролируемых исследований
По крайней мере, 1 рандомизированное контролируемое исследование
По меньшей мере, 1 контролируемое исследование без рандомизации
По крайней мере, 1 квази-экспериментальное исследование
Описательные исследования, такие как сравнительные исследования, корреляционные исследования или «случай-контроль» исследования
Отчет экспертного комитета или мнение и/или клинический опыт уважаемых авторитетов
Таблица П2 –Уровни убедительности рекомендаций
Уровень
Основания
Уровень доказательства 1
Уровень доказательства 2 или экстраполированные рекомендации уровня доказательства 1
Уровень доказательства 3 или экстраполированные рекомендации уровней доказательства 1 или 2
Уровень доказательства 4 или экстраполированные рекомендации уровней доказательства 2 или 3
Порядок обновления клинических рекомендаций - Каждые 3 года.
Приложение А3. Связанные документы
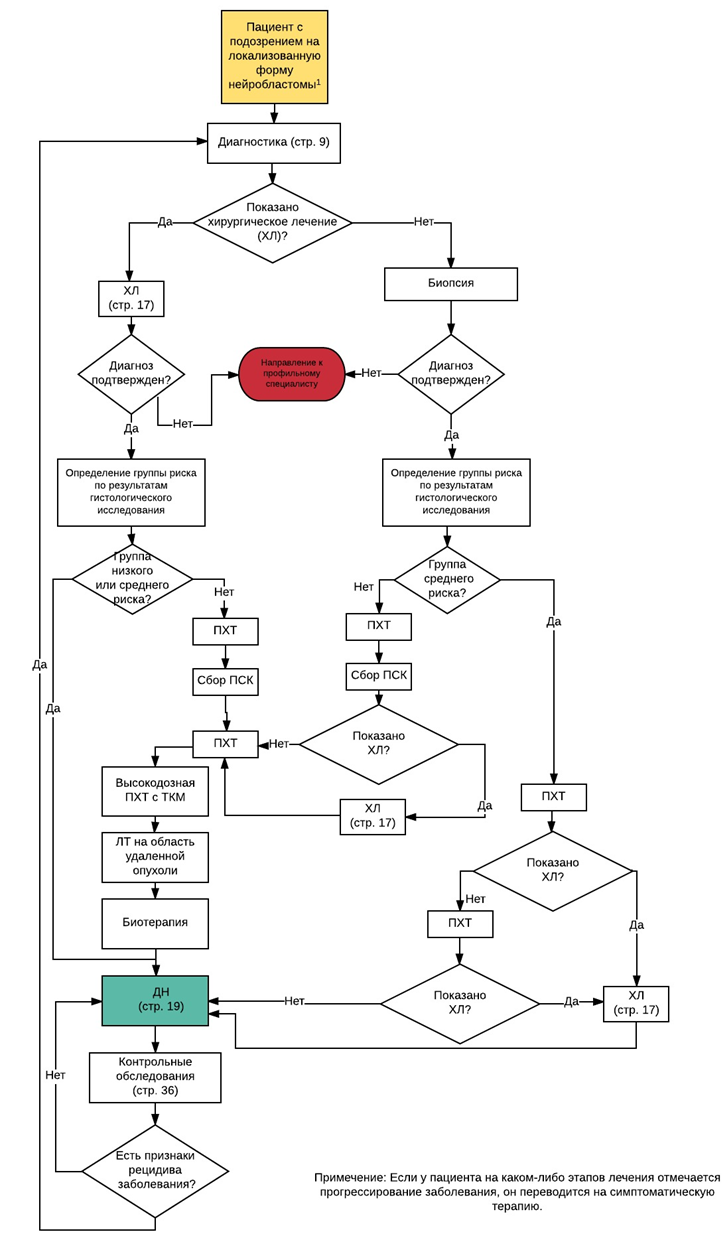
Приложение Б. Алгоритмы ведения пациента
2. Алгоритм обследования и лечения пациента с генерализованной формой нейробластомы
Приложение В. Информация для пациентов
Мукозит (стоматит) – поражение слизистой оболочки полости рта, приводящее к воспалению, а при тяжелых формах к болезненным язвам и инфекции. Эта тяжелая токсическая реакция, в которую могут быть вовлечены язык и десны. Наиболее часто стоматиты возникают, если в состав химиотерапии входят такие лекарства, как метотрексат, фторурацил, доксорубицин, блеомицин. Важно выявить стоматит на начальной стадии. Для этого во время курса ПХТ, потенциально вызывающей стоматит, необходимо каждое утро съедать дольку апельсина и, если во рту начинает «пощипывать», сообщить лечащему врачу.
Меры профилактики возникновения стоматита:
Признаки стоматита: «пощипывание», покраснение слизистой оболочки полости рта, обильное выделение слюны, болезненность при пережевывании пищи. Могут появиться пузырьки, отечность языка, жжение, дискомфорт.
Ниже приводим несколько советов, как справиться со стоматитом:
Диетические рекомендации при стоматитах:
Готовые смеси для детей (мясные, овощные и фруктовые), различные виды творога, йогурты, некислые желе, мягкие неострые сыры, взбитые сливки.
Включайте в рацион следующие блюда и напитки: овсяная каша, процеженный молочный суп, яйца всмятку, картофельное пюре, суп-пюре, творожный пудинг (можно размять с молоком), крем из яиц и молока и другую не раздражающую пищу. Не рекомендуется употреблять кислые фрукты и цитрусовые, так как они могут усилить раздражение слизистой оболочки полости рта. Используйте мягкую пищу, когда утихнут острых явлений стоматита. Готовьте тушеные, вареные, мятые блюда (мясо на пару, салаты с провернутым мясом и птицей, запеканки, суфле, пудинги, супы и бульоны с минимальным количеством соли и, естественно, без перца). Помидоры употребляйте с осторожностью, т.к. они обладают способностью усиливать раздражение слизистой оболочки полости рта. Многим помогает варенье из лепестков роз. Настоятельно рекомендуется при стоматитах сливочное и молочное мороженое без каких-либо добавок.
В тех случаях, когда у Вас появляется сухость или дискомфорт в полости рта или горле, когда пережевывание и глотание пищи затрудненно, попробуйте пить больше жидкости (до 2-х литров в день). Арбуз и дыня должны регулярно появляться на Вашем столе. Держите недолго во рту кусочки льда или не содержащие сахара леденцы и жевательные резинки.
Диетические мероприятия при диарее направлены на восстановление водно-минерального, витаминного и белкового равновесия. При этом пища должна максимально щадить слизистую оболочку кишечника. На первом этапе лечения кишечник нуждается в отдыхе, поэтому диета должна включать только мягкую и жидкую пищу (приготовленную на пару или вареную). Кроме того, в течение 3-5 дней желательно ограничивать калорийность пищи за счет уменьшения углеводов и жиров. Из диеты исключают жирные сорта мяса и рыбы, копчености, маринады, консервы, острые специи и раздражающие кишечный тракт овощи (редька, лук, редис, чеснок). Запрещаются бобовые, щавель, шпинат, кислые сорта ягод и фруктов, крепкие бульоны, жаренные и тушеные вторые блюда, свежее цельное молоко, а также мягкий хлеб, кондитерские изделия, блины, пирожки.
Дополнительно используйте следующие практические советы:
Диетологи рекомендуют пудинг из моркови, чернослива, яблок с добавлением лимона, свекольное пюре, винегрет с растительным маслом. По утрам натощак рекомендуется выпить стакан минеральной воды, фруктовый сок (сливовый, персиковый, абрикосовый) или горячий лимонный напиток. Послабляющее действие оказывают съеденные натощак тертая морковь, сырое яблоко, простокваша, 5-7 штук чернослива, вымытого и залитого с вечера кипятком. Кроме того, при общем удовлетворительном состоянии показаны прогулки и незначительная физическая нагрузка. Полезны утренняя гимнастика, физические упражнения с акцентом на мышцы живота, рекомендуются быстрая ходьба.
Лекарственная терапия запоров должна проводиться с большой осторожностью, кратковременными курсами, под строгим контролем врача.
Токсическое действие химиотерапии на кроветворение
Большинство противоопухолевых препаратов поражает костный мозг, снижая его способность производить кровяные клетки. К ним относятся форменные элементы крови – эритроциты, лейкоциты, тромбоциты. Действие на кроветворение является самым главным побочным явлением химиотерапии. Наиболее часто страдают лейкоциты, в меньшей степени тромбоциты, и еще реже повреждается красный кровяной росток – эритроциты. Противоопухолевые препараты наиболее активно действуют на быстро делящиеся опухолевые клетки. Так как лейкоциты имеют наиболее короткую продолжительность жизни, то поражаются они значительно чаще и в большей степени, чем другие элементы крови. Благодаря более медленному делению и длительному (по сравнению с лейкоцитами) сроку жизни эритроцитов, анемия из-за подавления эритроцитов встречается редко и не имеет серьезного клинического значения.
Как правило, лейкопения, нередко сопровождаемая тромбоцитопенией, возникает на 7-14 день от начала лечения с последующим восстановлением числа лейкоцитов к 21-28 дню. Контроль за показателями крови целесообразно продолжать и после окончания введения препаратов. Планируемый очередной курс химиотерапии может быть отложен до тех пор, пока число лейкоцитов не восстановится.
Главная опасность лейкопении – возможность развития инфекций. В этот период источником инфекционных заболеваний являются микробы, которые находятся как внутри организма, так и в окружающей среде.
Низкое число лейкоцитов может привести к маскировке классических симптомов воспаления, в частности, к отсутствию высокой температуры, что затрудняет диагностику инфекции. Признаки инфекции, которые должны насторожить родителей ребенка, получающего химиотерапию:
• Температура выше 38.
• Явления простуды (кашель, насморк, боли в горле).
• Повышенная потливость, особенно по ночам.
• Чувство жжения при мочеиспускании.
В случае появления описанных выше симптомов, сообщите об этом лечащему врачу.
Роль психологической поддержки при химиотерапии
Наибольшее значение имеют следующие факторы: общее влияние химиотерапии на организм, вызывающее многочисленные побочные явления и психические изменения: тревога, напряжение, страх, возбуждение, депрессия являются наиболее частыми реакциями для многих больных.
Не стесняйтесь задавать интересующие Вас вопросы лечащему врачу. Помните, что Ваше эмоциональное благополучие так же важно, как и физическое здоровье.