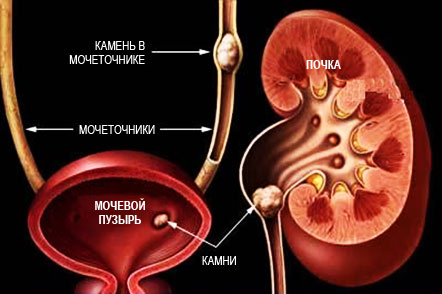
Нарушения обмена кальция
Рубрика МКБ-10: E83.5
Содержание
Определение и общие сведения [ править ]
Это гетерогенное нарушение, связанное с повышенным выделением кальция с мочой при кишечной гиперабсорбции (абсорбтивная гиперкальциурия) или сниженной реабсорбцией кальция в почечных канальцах (потеря через почки).
Этиология и патогенез [ править ]
Абсорбтивная гиперкальциурия возможна при первичной кишечной аномалии с гиперабсорбцией из-за повышенной реактивности кишки на кальцитриол (тип I) или повышенного содержания кальцитриола в крови (тип II). Повышение концентрации кальцитриола может быть причиной потери фосфатов через почки, что в последующем вызовет уменьшение содержания неорганического фосфора в сыворотке крови, повышенную продукцию кальцитриола, усиление кишечной абсорбции кальция, повышенную концентрацию кальция в сыворотке и гиперкальциурию (тип III). Первичная потеря кальция через почки нарушает его реабсорбцию в канальцах и также может вызвать гиперкальциурию (почечная гиперкальциурия). Идиопатическая гиперкальциурия может быть наследственной.
Клинические проявления [ править ]
Нарушения обмена кальция: Диагностика [ править ]
Концентрация неорганического фосфора в сыворотке понижена при абсорбтивной гиперкальциурии III типа в связи с первичной потерей фосфатов через почки. Концентрация ПТГ (паратгормона) при почечной гиперкальциурии повышается, потому что первичное нарушение состоит в снижении реабсорбции кальция, которое вызывает относительную гипокальциемию и стимулирует выход ПТГ по принципу обратной отрицательной связи. При абсорбтивной гиперкальциурии II типа содержание кальция в суточной моче нормальное, как и у больных, находящихся на диете с ограничением кальция (400 мг в день), потому что абсорбционный избыток не столь значительный. Тем не менее количество кальция в суточной моче при ограничении потребления кальция при абсорбтивной гиперкальциурии I и III типа, почечной гиперкальциурии остаётся высоким. Нормальная суточная экскреция кальция с мочой при ограничении кальция в пище до 400 мг в день составляет менее 200 мг/сут. Концентрация кальция в моче натощак в норме менее 0,11 мг/100 мл СКФ. Нормальное соотношение кальция и креатинина в моче меньше 0,2 после приёма 1 г кальция в качестве нагрузки.
Дифференциальный диагноз [ править ]
Установление типа идиопатической гиперкальциурии имеет важное значение для подбора адекватной медикаментозной терапии почечнокаменной болезни.
Нарушения обмена кальция: Лечение [ править ]
Лечение поддерживающее и включает в себя гидратацию и вывод из организма патогенных агентов.
Профилактика [ править ]
Прочее [ править ]
Молочно-щелочной синдром характеризуется гиперкальциемией, различной степенью почечной недостаточности и метаболическим алкалозом за счет приема большого количества кальция и абсорбции щелочи.
Точный патомеханизм молочно-щелочного синдрома остается неопределенным, предполагается, что имеет место взаимодействие между гиперкальциемией и алкалозом в почках, которые взаимно усиливают и поддерживают нарушение, приводящее к клинической картине синдрома.
Кальцифилаксия чаще всего встречается у пациентов с терминальной стадией почечной недостаточности, находящихся на гемодиализе или после трансплантации почки. До 4% пациентов на гемодиализе могут демонстрировать признаки кальцифилаксии, которые варьируются от болезненных подкожных узелов до неспецифических язв и гангрены конечностей.
Раннее выявление и мультидисциплинарное лечение кальцифилаксии, включая тщательный уход за раной с ее хирургической обработкой, паратиреоидэктомия и соответствующая трансплантация или реваскуляризация кожи, может улучшить заживление ран и спасти конечность.
Семейная гипокальциурическая гиперкальциемия
Синонимы: семейная доброкачественная гиперкальциемия, семейная доброкачественная гипокальциеральная гиперкальциемия
Определение и общие сведения
Семейная гипокальциурическая гиперкальциемия является обычно бессимптомным генетическим расстройством фосфорно-кальциевого метаболизма, характеризующаяся умеренной пожизненной гиперкальциемией, нормо- или гипокальциурией и повышенным содержанием паратиреоидного гормона (ПТГ) в плазме крови.
Распространенность семейной доброкачественной гиперкальциемии не известна. Семейная гипокальциурическая гиперкальциемия наследуется как аутосомно-доминантный признак.
Этиология и патогенез
Выделяют 3 генетических типа семейной гипокальциурической гиперкальциемии. Тип 1 (65% случаев) обусловлен инактивирующей мутацией в гене CASR (3q21.1), кодирующем кальций-чувствительный рецептор CaSR. Потеря функции рецептора CaSR приводит к снижению чувствительности клеток паращитовидной железы и почек к уровню кальция, поэтому гиперкальциемия воспринимается как нормальное состояние. Другие 35% случаев имеют либо мутацию гена GNA11 (19p13.3), наблюдаемую при 2 типе семейной гипокальциурической гиперкальциемии, либо AP2S1 (19q13.2-q13.3), наблюдаемую при 3 типе патологии, либо в генах, которые еще не были идентифицированы. В редких случаях семейная гипокальциурическая гиперкальциемия вызвана наличием аутоантител к кальций-чувствительному рецептору CaSR.
Предпологается, что если оба родителя имеют тип 1 семейной гипокальциурической гиперкальциемии, их потомство имеет более высокий риск развития неонатального тяжелого первичного гиперпаратиреоза.
Семейная гипокальциурическая гиперкальциемия характеризуется умеренной, но выявлямой гиперкальциемией, сопровождаемой неадекватными уровнями ПТГ и экскреции кальция с мочей: концентрация ПТГ в сыворотке обычно нормальна или слегка увеличены, а кальциурия низкая. Семейная гипокальциурическая гиперкальциемия обычно протекает бессимптомно, изредка отмечаются утомляемость, слабость, жажда и нарушения концентрации внимания. Некоторые взрослые пациенты имеют рецидивирующий панкреатит, хондрокальциноз и преждевременную кальцификацию сосудов.
Первичный гиперпаратиреоз клинически схож с семейной гипокальциурической гиперкальциемией, но для него не характерна гиперкальциемия. Дифференциальный диагноз включает также гуморальную злокачественную гиперкальциемию и саркоидоз.
Семейная гипокальциурическая гиперкальциемия не снижает ожидаемую продолжительность жизни и имеет благоприятное, стабильное течение.
Источники (ссылки) [ править ]
Mayo Clin Proc. 2009 Mar; 84(3): 261–267.
Hafner J, Keusch G, Wahl C, et al. Uremic small-artery disease with medial calcification and intimal hyperplasia (so-called calciphylaxis): a complication of chronic renal failure and benefit from parathyroidectomy. J Am Acad Dermatol 1995; 33:954.
Нарушения минерального обмена в почках (дисметаболические нефропатии)
Содержание
В зависимости от причины развития выделяют первичные и вторичные НМО.
Первичные нарушения представляют собой наследственно обусловленные формы заболеваний, характеризующихся прогрессирующим течением, ранним развитием мочекаменной болезни (МКБ) и хронической почечной недостаточности (ХПН). Первичные дисметаболические нефропатии встречаются редко и начало клинических проявлений развивается уже в детском возрасте.
Вторичные дисметаболические нефропатии могут быть связаны с повышенным поступлением определенных веществ в организм, нарушением их метаболизма в связи с поражением других органов и систем (например, желудочно-кишечного тракта), применением ряда лекарственных средств и др.
Оскалатно-кальциевая нефропатия
Оксалатно-кальциевая нефропатия наиболее часто встречается в детском возрасте. Ее возникновение может быть связано с нарушением обмена кальция или оксалатов (солей щавелевой кислоты).
Причины образования оксалатов:
Оксалатная нефропатия представляет собой многофакторный патологический процесс. Наследственная предрасположенность к развитию оксалатной нефропатии встречается в 70–75%. Помимо генетических, большую роль играют такие внешние факторы, как: питание, стресс, экологические проблемы и др.
Первые проявления болезни могут развиться в любом возрасте, даже в период новорожденности. Чаще всего они выявляются в 5–7 лет в виде обнаружения кристаллов оксалатов, небольшим содержанием белка, лейкоцитов и эритроцитов в общем анализе мочи. Характерно повышение удельной плотности мочи. Заболевание обостряется в период полового созревания в возрасте 10–14 лет, что, по-видимому, связано с гормональной перестройкой.
Фосфатная нефропатия
Фосфатная нефропатия встречается при заболеваниях, сопровождающихся нарушением фосфорного и кальциевого обмена. Основная причина фосфатурии – хроническая инфекция мочевой системы. Часто фосфатно-кальциевая нефропатия сопровождает оксалатно-кальциевую, но при этом выражена в меньшей степени.
Уратная нефропатия (нарушения обмена мочевой кислоты)
Эта группа обменных нарушений наиболее часто встречается у взрослых. Первичные уратные нефропатииобусловлены наследственными нарушениями обмена мочевой кислоты. Вторичные возникают как осложнениядругих заболеваний (болезней крови и др.), являются следствием применения некоторых препаратов (тиазидовых диуретиков, цитостатиков, салицилатов, циклоспорина А и др.) или нарушения функции канальцев почек и физико-химических свойств мочи (при воспалении почек, например). Кристаллы уратов откладываются в ткани почек – это приводит к развитию воспаления и снижению почечных функций.
Первые признаки заболевания могут выявляться в раннем возрасте, хотя в большинстве случаев наблюдается длительное скрытое течение процесса.
Цистиновая нефропатия
Цистин является продуктом обмена аминокислоты метионина. Можно выделить две основные причины повышения концентрации цистина в моче:
Накопление цистина в клетках происходит в результате генетического дефекта фермента цистинредуктазы. Это нарушение обмена носит системный характер и называется цистинозом. Внутриклеточное и внеклеточное накопление кристаллов цистина выявляется не только в канальцах и интерстиции почки, но и в печени, селезенке, лимфоузлах, костном мозге, клетках периферической крови, нервной и мышечной ткани, других органах. Нарушение обратного всасывания цистина в канальцах почек наблюдается вследствие генетически обусловленного дефекта транспорта через клеточную стенку для аминокислот – цистина, аргинина, лизина и орнитина.
По мере прогрессирования заболевания определяются признаки мочекаменной болезни, а при присоединении инфекции – воспаление почек.
Симптомы НМО
НМО почек, как правило, клинически течет бессимптомно до формирования мочекаменной болезни или пиелонефрита, но в ряде случаев могут проявляться следующими симптомами:
Диагностика НМО
Необходимое комплексное обследование включает лабораторные и инструментальные методы.
Лабораторная диагностика
Инструментальная диагностика
УЗИ органов брюшной полости. Изменения, выявляемые при УЗИ почек, как правило, мало специфичны. Возможно выявление в почке микролитов или «песка» (включений). УЗИ почек, как правило, является неспецифичным методом диагностики, однако в ряде случаев позволяет отследить формирование мелких камней и, таким образом, зафиксировать время возникновения мочекаменной болезни.
Лечение
Рекомендации по питанию являются основой терапии как в детском, так и во взрослом состоянии.
| Вид нефропатии | Запрещенные продукты |
| Оксалатная нефропатия | Мясные блюда, щавель, шпинат, клюква, свекла, морковь, какао, шоколад |
| Уратная нефропатия | Печень, почки, мясные бульоны, горох, фасоль, орехи, какао, алкогольные напитки |
| Фосфатная нефропатия | Сыр, печень, икра, курица, бобовые, шоколад |
| Цистиновая нефропатия | Творог, рыба, яйца, мясо |
Лечение оксалатной нефропатии
Лекарственная терапия включает мембранотропные препараты и антиоксиданты. Лечение должно быть длительным. Применяются витамины группы В, А, Е. Назначаются специальные препараты при кристаллурии. Помимо этого, назначается окись магния, особенно при повышенном содержании оксалатов.
Лечение уратной нефропатии
Для поддержания оптимальной кислотности мочи можно использовать цитратные смеси. При уратной нефропатии важно уменьшить концентрацию мочевой кислоты. Для этого используются средства, снижающие синтез мочевой кислоты.
Лечение фосфатной нефропатии
Назначается диета с ограничением продуктов, богатых фосфором (сыр, печень, икра, курица, бобовые, шоколад и др.).
Лечение при фосфатной нефропатии должно быть направлено на подкисление мочи (минеральные воды – нарзан, арзни, дзау-суар и др.; препараты – цистенал, аскорбиновая кислота, метионин).
При любой степени тяжести заболевания необходимо незамедлительно обратиться к врачу нефрологу или урологу за помощью, так как длительно текущие, в целом обратимые, нарушения обмена при отсутствии лечения могут привести к развитию мочекаменной болезни с последующим оперативным вмешательством и хронической почечной недостаточности. Самолечение не допустимо!
Все виды лекарственной терапии должен назначать и обязательно контролировать врач нефролог или уролог, так как:
На первом этапе лечения составляется план лечения. Лечение любой дисметаболической нефропатии можно свести к четырем основным принципам:
Прием большого количества жидкости является универсальным способом лечения любой дисметаболической нефропатии, так как способствует уменьшению концентрации растворимых веществ в моче.
Одной из целей лечения является увеличение ночного объема мочеиспускания, что достигается приемом жидкости перед сном. Предпочтение следует отдавать простой или минеральной воде.
Диета позволяет в значительной степени снизить солевую нагрузку на почки.
Специфическая терапия должна быть направлена на предупреждение конкретного кристаллообразования, выведение солей, нормализацию обменных процессов.
На втором этапе терапии производится оценка эффективности диеты, проводятся контрольные УЗ-исследования и анализы.
Третий этап лечения осуществляется после достижения стойкой ремиссии. Он представляет собой схему постепенного снижения доз назначенных препаратов до поддерживающих или полной их отмены с сохранением диетических рекомендаций.
Даже после достижения долгожданной ремиссии пациенту рекомендуется быть внимательным к себе и регулярно наблюдаться у врача нефролога или уролога, так как высок риск рецидива заболеваний.
Практически всем пациентам необходимо принимать рекомендованные врачом средства противорецидивной терапии или придерживаться ранее разработанной диеты для предотвращения формирования или прогрессирования МКБ, воспаления почек.
Прогноз
Прогноз при дисметаболической нефропатии в целом благоприятен. В большинстве случаев при соответствующем режиме, диете и лекарственной терапии удается добиться стойкой нормализации соответствующих показателей в моче. В отсутствие лечения или при его неэффективности наиболее естественным исходом дисметаболической нефропатии является мочекаменная болезнь и воспаление почек.
Самым частым осложнением дисметаболической нефропатии является развитие инфекции мочевой системы, в первую очередь пиелонефрита.
Если вы обнаружили у себя какие-либо из перечисленных выше симптомов (нарушение мочеотделения, изменения свойств мочи, боли), необходимо в ближайшее время обратиться к врачу за помощью.
Помните, что очень важно начать лечение на ранних стадиях болезни, так как НМО в почках является преимущественно обратимым состоянием, а в случае отсутвтия лечения итогом является развитие мочекаменной болезни, пиелонефрита.
Рекомендации
Для профилактики развития заболевания, а так же рецидива, необходимо придерживаться правильного, сбалансированного и регулярного питания – избегать острой пищи, маринадов и пр. В период обострения пациентам рекомендуется щадящая диета, соответствующая требованиям биохимического вида нефропатии (оксалатная, уратная и пр.).
С целью профилактики рецидивов всем пациентам рекомендуется один раз в квартал консультация врача нефролога или уролога для необходимой коррекции медикаментозной терапии и пищевых рекомендаций.
Пациенты, длительно страдающие НМО в почках, относятся к группе повышенного риска по МКБ. Поэтому в период ремиссии им необходимо ежегодно проходить по назначению врача контрольные обследования (общий анализ мочи, биохимия мочи, УЗИ почек, мочеточников, мочевого пузыря) мочевыводящей системы.
Часто задаваемые вопросы
Излечимы ли НМО?
НМО часто обусловлено наследственными нарушениями обмена, что требует постоянного соблюдения как минимум диетических рекомендаций.
Из-за чего возникает заболевание?
НМО может быть связано с наследственной предрасположенностью, а также с заболеваниями внутренних органов (желудочно-кишечные проблемы, заболевания крови и пр.), применением определенных групп лекарственных препаратов (мочегонные средства, цитостатики и пр.).
Является ли заболевание противопоказанием к беременности?
Само НМО в почках требует наблюдения весь период беременности с соблюдением диетических рекомендаций.
При развитии МКБ, пиелонефрита и их осложнений в виде ХПН, возможность беременности и ее сохранения зависит от обострения процесса и стадии осложнений и решается в каждом конкретном случае.
Может ли заболевание почек проявляться снижением потенции?
Непосредственно НМО конечно не влияет на потенцию, но в случае развития осложнений МКБ, воспаления почек или развития ХПН снижение потенции может появиться как реакция на хроническое заболевание.
Увеличивается ли риск заболеть, если близкий родственник страдает данным заболеванием?
Да, существует группа первичных обменных нефропатий (НМО в почках), имеющая наследственную предрасположенность.
Рахит
Общая информация
Краткое описание
Название протокола: Рахит
Рахит – это группа заболеваний детского организма, связанная с недостаточным поступлением витамина D или нарушением процессов его метаболизма, приводящая к нарушению многих видов обмена веществ и в первую очередь фосфорно- кальциевого(КФО), что обусловливает поражение многих органов и систем, но главным образом, костного скелета (Майданник В.Г., 2014 г).
Витамин D-дефицитный рахит – заболевание интенсивно растущего детского организма, обусловленное нарушением регуляции КФО и минерализации костной ткани в результате дефицита витамина D (Майданник В.Г., 2014 г)
Код протокола:
Код(ы) МКБ-10:
Е55 Рахит активный
Сокращения, используемые в протоколе:
Дата разработки протокола: 2015 год.
Категория пациентов: дети.
Пользователи протокола: врач скорой помощи, фельдшер, врач общей практики, педиатр.
Оценка на степень доказательности приводимых рекомендаций.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортных или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
| Тяжесть | Течение | Период |
| I легкая II средней тяжести III тяжелое | Острое Подострое Рецидивирующее | Начальных проявлений Разгара Реконвалесценции Остаточных изменений |
Вторичный рахит часто возникает:
· присиндромахмальабсорбции;
· при хронических болезнях почек или желчевыводящих путей;
· приболезняхобменавеществ (тирозинемия, цистинурия и др.);
· вызванныйдлительнымприменениемпротивосудорожныхсредств (дифенин, фенобарбитал), диуретиков, глюкокортикоидов, а также, парентеральнымпитанием.
Витамин D-зависимый рахит:
· Тип I — генетический дефект синтеза в почках 1,25-дигидроксивитамина D — 1,25(OH)2D.
· Тип II — генетическая резистентность рецепторов органов-мишеней к 1,25(OH)2D.
Витамин D-резистентный рахит:
· Фосфат-диабет;
· Синдром де Тони — Дебре — Фанкони (de Toni-Debré-Fanconi);
· Гипофосфатазия;
· Почечный тубулярный ацидоз.
Клиническая картина
Cимптомы, течение
Диагностические критерии [1,8-10]:
Жалобы и анамнез:
Жалобы: беспокойство, пугливость, раздражительность, гиперестезия, снижение аппетита, нарушение сна, вздрагивание при засыпании, громком звуке, вспышке света; повышенная потливость, ребенок трет голову о подушку, облысение затылка;деформация костей головы, грудной клетки, позвоночника, конечностей; отставание в физическом развитии, запаздывание прорезывания зубов
Анамнез: заболевание выявляется с 3-4 месячного возраста, хотя первые симптомы могут появиться в 1 – 1,5 месяца. Выявление факторов риска
Физикальное обследование:
Клинические критерии:
· Симптомы остеомаляции (размягчение, обеднения кальцием кости – преобладают при остром течении рахита) – податливость костей черепа, краев родничка, краниотабес, брахицефалия, деформация костей черепа, конечностей, ключиц, плоский таз, эрозии и кариес зубов.
· Симптомы остеоидной гиперплазии (преобладают при подостром течении рахита) – лобные и теменные бугры, реберные «четки», надмыщелковые утолщения голеней, «браслетки» на предплечьях, «нити жемчуга» на пальцах.
· Симптомы гипоплазии костной ткани – задержка роста с характерной «коротконогостью», позднее прорезывание молочных и постоянных зубов, позднее закрытие родничка.
· Симптомы мышечной гипотонии – искривление позвоночника со спино-поясничным кифозом, сколиозом, деформацией грудной клетки с развернутой нижней апертурой, вялость и дряблость мышц, разболтанность суставов, «лягушачий» живот.
· Задержка статических и локомоторных функций.
I – лёгкая– соответствует начальному периоду рахита.
Незначительные нарушения общего состояния: нервная возбудимость, беспокойство, вздрагивания при резком звуке, вспышке света, нарушения ритма сна, поверхностный «тревожный» сон. Потливость (липкий пот с кислым запахом), зуд кожи, ребенок трет затылком о подушку, что приводит к облысению затылка. Со стороны костной системы: податливость краев большого родничка.
II – средней тяжести — умеренно выраженные изменения костной системы и внутренних органов.отчётливые деформации черепа, грудной клетки, небольшое увеличение печени и селезёнки, умеренная анемия;
· со стороны ЦНС – задерживается развитие статических и локомоторных функций, позже начинает поднимать голову, сидеть, вставать и ходить, пассивные движения обычно вызывают у них отрицательную реакцию, нарушается поведение, сон, аппетит;
· со стороны мышечной системы– выраженная мышечная гипотония и слабость связочного аппарата: в положении на спине легко притягивают ногу к голове, сосут первый палец на стопе, кладут стопу на плечо; большой, распластанный «лягушачий» живот, дряблость мышц брюшной стенки; расхождение прямых мышц живота; предрасположенность к воспалению легких, выявляются дистрофические изменения в сердце;
· гипохромная анемия, преимущественно железодефицитная, но может быть вследствие дефицита аминокислот, меди и цинка;
· со стороны костной ткани:
симптомы остеоидной гиперплазии: лобные и теменные бугры, реберные «четки», надмыщелковые утолщения голеней, «браслетки» на запястьях, «нити жемчуга» на пальцах;
· симптомы гипоплазии костной ткани: задержка роста из-за отставания роста трубчатых костей в длину, позднее прорезывание молочных и постоянных зубов, позднее закрытие родничков, плоский таз;
· костные деформации: деформации грудной клетки с развернутой нижней апертурой, «гаррисонова борозда», килевидная («куриная» грудь) или воронкообразная («грудь сапожника») деформация.
III – тяжёлая – поражение нескольких отделов костной системы, тяжёлое поражение внутренних органов и нервной системы, отставание в физическом и психическом развитии, деформация нижних конечностей – О-образное (genuvarum), X-образное (genuvalgum) и другие (coxavara, genurecurvatum). Искривления позвоночника в виде сколиоза, лордоза, поясничного кифоза.
Начальный период наиболее чётко начинает проявляться в возрасте 3-4 месяцев, однако первые симптомы могут возникать и раньше – в 1-1,5 месяца, но они не специфичны и часто могут проходить мимо внимания родителей. На первое место выступают неврологические и вегетативные изменения. Ребёнок проявляет беспокойство, капризность, нарушается сон –дети плохо засыпают и часто просыпаются, появляется пугливость, раздражительность, дети часто вздрагивают от громкого звука или яркого света. Заметно снижается аппетит – ребёнок с неохотой и на короткое время берёт грудь, вялососёт – иногда бывают запоры. Кроме того, обращают на себя внимания такие вегетативные проявления как потливость, особенно во сне, и повышение сосудистой возбудимости кожи, которое проявляется в виде усиления интенсивности и длительности красного дермографизма. Наиболее интенсивно, вызывая у ребёнка сильный зуд, потеет волосистая часть головы, которой ребёнок постоянно трётся о подушку, это и приводит к специфичному для рахита облысению затылка. Также обращает на себя внимание характерный резкий и кислый запах пота. Возможно некоторое снижение тонуса мышц ребёнка. Костные изменения для начального периода рахита не характерны, однако иногда может обнаруживаться некоторая податливость краёв большого родничка. Начальный период болезни длится, как правило, от 2 до 4 недель.
В период разгара прогрессируют изменения костной системы: остеомаляция грудной клетки, нижних конечностей, избыточный остеогенез (рахитические «чётки», «браслетки», лобные и теменные бугры черепа). Ребёнок может отставать в физическом и психическом развитии.
При рахите тяжелой степени нарушены функциональное состояние печени, желудочно – кишечного тракта, белковый, липидный обмен, имеется дефицит витаминов В1, В6, В5, А, Е, С, меди, цинка, магния.
У большинства детей с рахитом 1 и 2 степени наблюдаются явления гипохромной анемии.
В период реконвалесценции (выздоровления) постепенно исчезают клинические и лабораторные симптомы рахита. Возникшие при рахите деформации скелета остаются и вовзрослом возрасте: нарушение осанки, изменения грудной клетки, костей нижних конечностей. Перенесенный рахит может способствовать поражению зубов ( развитию множественного кариеса), развитию близорукости, плоскостопия, сужению, деформации костей таза.
· Острое течение – бурное развитие всех симптомов, яркие неврологические и вегетативные расстройства, значительнаягипофосфатемия, высокий уровень ЩФ, преобладание процессов остеомаляции.
· Подострое течение – свойственны умеренно выраженные или малозаметные неврологические и вегетативные нарушения, превалирование процессов остеоидной гиперплазии.
· Рецидивирующее течение – типичны смены периодов обострения и стихания процесса с сохраняющимися остаточными явлениями. При рентгенографии зон роста обнаруживается несколько полос обызвествления в метафизах.
Диагностика
Диагностические исследования:
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне:
· ОАК;
· ОАМ;
· определение в крови уровня кальция и фосфора;
· активность ЩФ в сывороткекрови;
· проба по Сулковичу (качественное определение степени кальциурии).
Дополнительные диагностические обследования, проводимые на амбулаторном уровне:
· Концентрация 25(ОН)Dв сыворотке крови(основной тест для определения уровня дефицита витаминаD).
· Рентгенорафия костей (при выраженных костных изменениях для дифференциальной диагностики).
· Денситометрия(для дифференциальной диагностики- степени определения остеопороза).
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне (при экстренной госпитализации):
· ОАК (контроль по показаниям- при наличии патологических изменений в анализе при поступлении);
· ОАМ (контроль по показаниям-при наличии патологических изменений в анализе при поступлении);
· биохимический анализ крови (кальций, фосфор, ЩФ);
· анализ мочи по Сулковичу
Дополнительные диагностические обследования, проводимые на стационарном уровне:
· ЭЭГ – при спазмофилии для дифференцировки с эпилепсией.
· Эхокардиографияи ЭКГ – при появлении симптомов нарушения сердечной деятельности.
Рентгенография костей (при выраженных костных изменениях для дифференциальной диагностики с другими рахитопобобными заболеваниями).
Показания для консультации узких специалистов:
· консультации узких специалистов (по показаниям) – сопутствующие соматические заболевания и\или патологические состояния.
Лабораторная диагностика
:
строгой корреляции между клиническими признаками рахита и лабораторными изменениями нет, так только у 50% детей с гиповитаминозом D наблюдается полное соответствие биохимических и рентгенологических данных (Мальцев С.В.,1987 г).
· Концентрация фосфора в сыворотке крови может снижаться до 0,65-0,8 ммоль/л (при норме у детей до 1 года 1,5-1,8 ммоль/л).
· Концентрация кальция – до 2,0-2,2 ммоль/л (при норме 2,2-2,7 ммоль/л).
· Концентрация ионизированного кальция менее 1.0 ммоль\л.
· Соотношение между уровнями кальция и фосфора в сыворотке крови в норме равное 2:1, в период разгара рахита повышается до 3:1-4:1. В начальном периоде рахита и в периоде разгара остеомаляционных явлений количество кальция может быть нормальным.
· ПовышениеактивностиЩФ в сыворотке крови в 1.5-2 раза ( абсолютные показатели нормы зависят от метода её определения).
· Снижение 25-ОН-Д в крови (в норме 20 нг\мл)снижение до 10 нг/мл свидетельствует о дефиците витамина D, а содержание ниже 5 нг/мл об авитаминозе (ІІ В).
| Критерии оценки статуса обеспеченности витамином Д на основании концентрации 25(ОН)Дtotal в сыворотке крови Practical guidelines for supplementation of Vitamin D and treatment of deficits in Central Europe, 2013 г. | |
| Концентрация 25(ОН)Дtotal в сыворотке, нг/мл (нмоль/л), 1 нг/мл=2,5 нмоль/л | Клиническаяинтерпретация |
| менее 20 нг/мл (50) | отражает дефицит витамина Д; требует медикаментозного лечения. |
| 20-30 нг/мл (50-70) | отражает субоптимальный статус обеспеченности витамином Д; требует умеренного повышения дневной дозы витамина Д. |
| 30-50 нг/мл(75-125) | отражает адекватный статус обеспеченности витамином Д; требует сохранения применяемой схемы обеспечения витамином Д и принимаемой дозы. |
| 50-100 нг/мл (125-250) | отражает высокий уровень поступления витамина Д; требует поддержания принимаемой дозы обеспечения витамином Д при низких значениях этого интервала или умеренного снижения дозы – при высоких значениях интервала. |