Нарушение обмена веществ неуточненное
Рубрика МКБ-10: E88.9
Содержание
Определение и общие сведения [ править ]
Синонимы: метаболический синдром X, синдром Reaven, синдром резистентности к инсулину
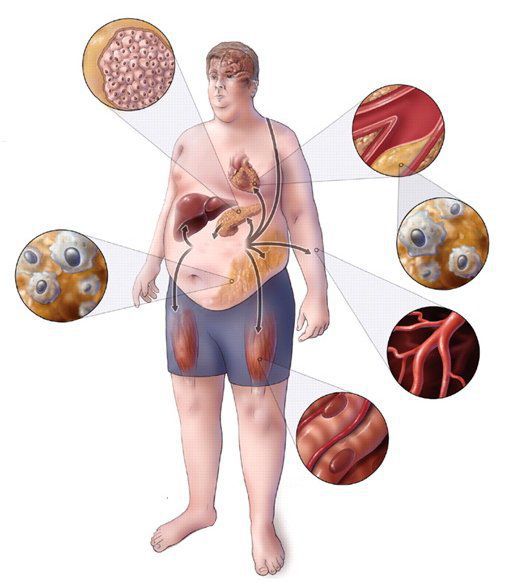
Метаболический синдром, характеризующийся генетически обусловленным нарушением липидного и углеводного обмена и ускоряющий развитие атеросклероза, сахарного диабета 2 типа и артериальной гипертензии, включает в себя, по заключению экспертов рабочей группы ВОЗ (1998), висцеральное (абдоминальное) ожирение, инсулинорезистентность, инсулинемию, нарушение толерантности к глюкозе (НТГ) или сахарный диабет 2 типа, артериальную гипертензию, дислипидемию, нарушения гемостаза, гиперурикемию и микроальбуминурию.
Этиология и патогенез [ править ]
J. Reaven, который в 1988 г. впервые выдвинул гипотезу о «Х-синдроме», связывал развитие клинических появлений этого сложного синдрома метаболических нарушений с инсулинорезистентностью и компенсаторной гиперинсулинемией, развивающейся в ответ на инсулинорезистентность. В связи с этим в последующем для обозначения совокупности метаболических расстройств многие исследователи начали использовать термин «синдром инсулинорезистентности» или «метаболический инсулинорезистентный синдром». К настоящему времени установлено, что инсулинорезистентность с нарушением чувствительности периферических тканей к инсулину наследуется и наиболее часто проявляется в среднем и пожилом возрасте, что связывают с возрастным повышением активности гипоталамических центров.
Генетическая предрасположенность к инсулинорезистентности объясняется мутацией генов: инсулинрецепторного субстрата I (инсулинрецепторная тирозинкиназа), гликоген-синтетазы, глюкозных транспортеров II или IV, гексокиназы II, белка, связывающего свободные жирные кислоты (FABP-II).
Одновременно с этим обсуждается предположение, согласно которому инсулинорезистентность является не причиной метаболического синдрома, а лишь одним из его проявлений. Это подтверждается результатами ряда проспективных исследований, свидетельствующих о том, что гиперинсулинемия является самостоятельным атерогенным фактором. Эти данные позволили предположить иной генетический фактор возникновения метаболического синдрома, получивший название «фактор Z». Этот гипотетический фактор, взаимодействуя с инсулинчувствительными тканями, эндотелием, регулирующей системой артериального давления и обменом липидов и липопротеинов, вызывает соответственно резистентность к инсулину, артериальную гипертензию, атерогенную дислипидемию и атеросклероз.
Хотя одним из клинических признаков метаболического синдрома принято считать ожирение, при котором отношение окружности талии к окружности бедер превышает 0,95 у мужчин и 0,85 у женщин, роль ожирения до последнего времени оставалась однозначно неопределенной. Инсулинрезистентность нередко обнаруживается у людей, не имеющих избыточной массы тела. Исследования последних лет, в которых, помимо антропометрических измерений, применялась компьютерная или магнитно-ядерная томография позволившие визуализировать и измерять жировые депо различной локализации, во многом прояснили вопрос. Стало понятным, что при отсутствии антропометрических признаков ожирения инсулинорезистентности сопутствует нарушение распределения жировой ткани с ее накоплением в висцеральных депо внутри брюшной полости, т. е. висцеральным ожирением. Обнаружена тесная коррелятивная связь между количеством висцерального жира и возрастом. Наиболее высокая взаимосвязь этих показателей выявлена у мужчин старше 50 лет и женщин старше 60 лет.
Согласно современной концепции патофизиологической основой метаболического инсулинорезистентного синдрома являются гормональные расстройства: инсулинорезистентность, гиперинсулинемия, избыток кортизола, не только уменьшающего инсулинообусловленный транспорт глюкозы в клетки, но и тормозящего пострецепторную утилизацию глюкозы, недостаточность андрогенов (у мужчин) и гормона роста. К провоцирующим влияниям относят стресс, курение, гиподинамию, высококалорийное питание с большим количеством легкоусвояемых углеводов и животных жиров. Провоцирующие факторы через нарушения секреции и действия гормонов приводят к метаболическим последствиям, прежде всего к гипергликемии, повреждениям эндотелия (эндотелиопатии), гиперхолестеринемии и атерогенной дислипидемии. Избыточное накопление висцерального жира скорее всего относится как к провоцирующим факторам, так и к патофизиологическим расстройствам, которые наряду с инсулинорезистентностью и гиперинсулинемией формируют патогенетическое ядро метаболического инсулинорезистентного синдрома.
Клинические проявления [ править ]
Нарушение обмена веществ неуточненное: Диагностика [ править ]
Дифференциальный диагноз [ править ]
Нарушение обмена веществ неуточненное: Лечение [ править ]
В первую очередь лечение должно быть направлено на решение проблемы избыточного веса, которое достигается, главным образом, немедикаментозными методами. Необходимо увеличить двигательную активность, уменьшить калорийность питания и рационализировать состав потребляемой пищи.
Фармакотерапия метаболического синдрома направлена на лечение ожирения, нарушений углеводного обмена, артериальной гипертонии и дислипидемии.
Что такое метаболический синдром? Причины возникновения, диагностику и методы лечения разберем в статье доктора Чернышев А. В., кардиолога со стажем в 26 лет.
Определение болезни. Причины заболевания
Метаболический синдром (синдром Reaven) представляет собой симптомокомплекс, сочетающий в себе абдоминальное ожирение, инсулинорезистентность, гипергликемию (повышенное содержание глюкозы в крови), дислипидемию и артериальную гипертензию. Все эти нарушения связаны в одну патогенетическую цепь. Кроме того, такой синдром часто сочетается с гиперурикемией (избытком мочевой кислоты в крови), нарушением гемостаза (свёртываемости крови), субклиническим воспалением, синдромом обструктивного апноэ-гипопноэ сна (остановкой дыхания во сне). [4]
Метаболический синдром – хроническое, распространённое (до 35% в российской популяции), полиэтиологическое заболевание (возникающее по многим причинам), в котором главная роль принадлежит поведенческим факторам (гиподинамия, нерациональное питание, стресс). Имеет значение также наследственная предрасположенность к артериальной гипертензии, атеросклероззависимым заболеваниям и сахарному диабету второго типа. [5]
Практикующим врачам важно выделять группу риска метаболического синдрома. К данной группе относятся пациенты с начальными признаками заболевания и его осложнениями: артериальная гипертензия, углеводные изменения, ожирение и повышенное питание, ишемическая болезнь сердца, атеросклеротические заболевания периферических и мозговых артерий, нарушение пуринового обмена, жировая болезнь печени; синдром поликистозных яичников; постменопаузальный период у женщин и эректильная дисфункция у мужчин; гиподинамия, злоупотребление алкоголем, табакокурение, наследственная отягощенность по сердечно-сосудистым и обменным заболеваниям. [3] [7]
Симптомы метаболического синдрома
Клинические проявления метаболического синдрома соответствуют симптомам его составляющих:
Если изменения составляющих синдрома Reaven носят субклинический характер (что встречается довольно часто), то и течение заболевания носит асимптомный характер.
Патогенез метаболического синдрома
Инсулинорезистентность — первопричина развития метаболического синдрома. Представляет собой нарушение утилизации глюкозы в органах-мишенях (поперечнополосатой мускулатуре, липоцитах и печени), связанное с дисфункцией инсулина. Инсулинорезистентность уменьшает усвоение и поступление в клетки скелетной мускулатуры глюкозы; стимулирует липолиз и гликогенолиз, что приводит к липидным и углеводным патологическим изменениям. Кроме того, инсулинорезистентность усиливает секрецию инсулина, в результате чего возникает компенсаторная гиперинсулинемия и активация эндокринных систем (симпатоадреналовой, ренин-ангиотензин-альдостероновой) с формированием артериальной гипертензии, дальнейшим нарушением метаболических процессов, гиперкоагуляции, субклинического воспаления, дисфункции эндотелия и атерогенеза. Эти изменения, в свою очередь, способствуют усилению инсулинорезистентности, стимулируя патогенетический «порочный круг».
Классификация и стадии развития метаболического синдрома
Чёткой классификации и стадийности метаболического синдрома не существует. Его деление некоторыми авторами на полный, включающий все составляющие синдрома, и неполный представляется необоснованным. Несмотря на это, выраженность симптомов, количество компонентов синдрома Reaven и наличие осложнений оказывают влияние на стратификацию риска и выбор тактики лечения у конкретного пациента. Для этого следует учитывать:
В зависимости от индекса массы тела (ИМТ), который рассчитывается делением веса (кг) на рост (м 2 ), классифицируются следующие типы массы тела (МТ):
Второй тип ожирения является более патогенным в плане риска возникновения сердечно-сосудистых заболеваний и сахарного диабета. Это связано с ожирением внутренних органов, в том числе печени (висцеральное ожирение, неалкогольная жировая болезнь печени), снижением сатурации крови кислородом из-за перехода дыхания на грудной, поверхностный тип и эндокринной активностью висцеральной жировой ткани с патологическим изменением выработки адипокинов (лептин, грелин, адипонектин). Выявлена чёткая корреляция между увеличением абдоминальной жировой ткани и индекса массы тела с риском сопутствующих заболеваний. Считается, что риски начинают нарастать при увеличении окружности талии (ОТ) >80 см у женщин и 94 см у мужчин, а при ОТ >88 см и 102 см соответственно риск возрастает значительно.
Центральным патологическим звеном метаболического синдрома является изменение углеводного обмена. Концентрацию глюкозы оценивают в капиллярной крови (норма 1
жен. >1,2
Осложнения метаболического синдрома
Диагностика метаболического синдрома
Для диагностики метаболического синдрома необходимо выявить у пациента основной признак — абдоминальное ожирение по измерению ОТ (>80 см у женщин и >94 см у мужчин) и хотя бы два дополнительных критерия, которые включают в себя:
В клинических условиях нужно дифференцировать метаболический синдром от механического сочетания факторов риска, например артериальной гипертензии, избыточной массы тела без признаков абдоминального ожирения и повышения уровня ОХ крови, что встречается довольно часто (до 30%). В сомнительных случаях рекомендовано дополнительное определение инсулинорезистентности по следующим методикам:
Лечение метаболического синдрома
Лечение метаболического синдрома следует разделить на немедикаментозное и медикаментозное.
Медикаментозное лечение метаболического синдрома, в зависимости от наличия тех или иных его компонентов, может включать гиполипидемические, антигипертензивные препараты, медикаменты для снижения инсулинорезистентности, постпрандиальной гипергликемии и веса.
Основными препаратами, которые используют при лечении артериальной гипертензии у больных синдромом Reaven и сахарным диабетом, являются ингибиторы ангиотензинпревращающего фермента, сартаны и агонисты имидазолиновых рецепторов. Однако для достижения целевого уровня артериального давления часто необходимо сочетание различных классов медикаментов, таких как пролонгированных блокаторов медленных кальциевых каналов, высокоселективных бета-адреноблокаторов и тиазидоподобных диуретиков (индапамид) в сочетании с медикаментами первой линии. [10]
При неэффективности монотерапии статинами целесообразно присоединение эзетрола в дозе 10 мг/сут, который препятствует всасыванию ОХ в кишечнике и может усиливать снижение ХС-ЛПНП на 15-20%.
Фибраты — ещё один класс липидснижающих препаратов. Они расщепляют богатые триглицеридами жировые частицы, снижают синтез свободных жирных кислот и повышают ХС-ЛПВП путём увеличения распада ЛНП. Это приводит к значительному уменьшению триглицеридов (до 50%), ХС-ЛПНП (до 20%) и увеличению ХС-ЛПВП (до 30%). Фибраты также имеют плейотропные эффекты: снижают концентрацию мочевой кислоты, фибриногена и улучшают инсулиночувствительность, однако их положительное влияние на прогноз пациентов не доказано. Наиболее эффективный и безопасный препарат этой группы — фенофибрат 145 мг/сут.
Для снижения инсулинорезистентности препаратом выбора является метформин, который обладает доказанным положительным эффектом на тканевую инсулинорезистентность через усиление поглощения глюкозы тканями-мишенями. Метформин уменьшает скорость всасывания углеводов в тонкой кишке, оказывает периферическое анорексигенное действие, уменьшает продукцию глюкозы печенью, улучшает транспорт глюкозы внутри клеток. Положительное воздействие метформина (1500-3000 мг/сутки) на конечные точки обусловлено снижением инсулинорезистентности, системными метаболическими эффектами (снижение веса, липидных нарушений, факторов свёртываемости крови и т.д.). [9]
При наличии у пациента с синдромом Reaven сахарного диабета второго типа могут применяться современные классы сахароснижающих препаратов, такие как аналог глюкагоноподобного пептида-1, ингибитор дипептидилпептидазы-4 и ингибитор натрийзависимого переносчика глюкозы второго типа. Представитель последнего класса эмпаглифлозин (Джардинс) в исследовании EMPA-REG OUTCOME (2016 год) снизил сердечно-сосудистую смертность у больных сахарным диабетом второго типа на 36%.
Медикаментозная коррекция морбидного ожирения показана, если немедикаментозное лечение не приводит к снижению массы тела более чем на 5% от исходного. Препараты для лечения ожирения делятся на аноретики центрального действия (сибутрамин), и средства, воздействующие на желудочно-кишечный тракт, например орлистат (Ксеникал).
Препарат для снижения аппетита сибутрамин в меньшей степени воздействует на дофаминовые и холинергические процессы, но уменьшает потребление жиров и углеводов, что приводит к похудению и улучшает жировой и углеводный метаболизм. Артериальное давление и частота сердечных сокращений при этом повышается только на 5%.
Орлистат является ингибитором желудочной и панкреатической липаз, вследствие чего треть пищевых триглицеридов не всасывается и снижается их концентрация в крови, что приводит к уменьшению калоража пищи и веса. Кроме того, снижается артериальное давление, уровень глюкозы и инсулинорезистентности.
В медицинской практике лечение метаболического синдрома зависит от наличия и выраженности его компонентов. В таблице ниже показана тактика подбора терапии при вариантах синдрома Reaven, которые встречаются наиболее часто.
Морбидное ожирение. Метаболический синдром
Общая информация
Краткое описание
• 30 кг/м 2 и выше — ожирение.
Бариатрический эффект выражается в (Exess weight loss – EWL%) – процентах потери лишнего веса в кг от избыточной массы тела.
Смешанный тип операции – бариатрический эффект достигается комбинированным путем: рестриктивной операцией на желудке и за счет снижения всасывательной поверхности желудочно-кишечного тракта.
Пользователи протокола: хирург, врач общей практики, терапевт, эндокринолог, кардиолог, гастроэнтеролог, гепатолог, невропатолог.
В данном протоколе используются Оксфордская система «доказательной медицины»[1], с уровнями доказательности (таблица 1), которые определяется при анализе научной литературы, и выборе степени рекомендации (таблица 2), которая в свою очередь зависит от уровня доказательности. В 2010 году в совместно выработанном клиническом руководстве Американская Ассоциация клинических эндокринологов, Общество бариатрических и метаболических хирургов использовали для оценки доказательной базы схожую оксфордской системе градацию уровня доказательности [2].
Таблица 1. Уровни доказательности
Следует отметить, что при определении степени рекомендации нет прямой связи между уровнем доказательности данных и степенью рекомендации. Данные рандомизированных контролируемых исследований не всегда ранжируются как степень рекомендаций А в случае, если имеются недостатки в методологии или разногласия между опубликованными результатами нескольких исследований. Также отсутствие доказательств высокого уровня не исключает возможности дать рекомендации уровня А, если имеется богатый клинический опыт и достигнут консенсус. Кроме того, могут быть исключительные ситуации, когда нельзя провести подтверждающие исследования, возможно, по этическим или другим причинам, и в этом случае точные рекомендации считаются полезными.
Метаболический синдром, диабет и сердечно-сосудистые заболевания



Международные названия
Содержание
ТЕРМИНОЛОГИЯ СОГЛАСНО МКБ-10
Метаболический синдром представляет собой кластер четырех кардиометаболических факторов риска, которые согласно МКБ-10 определены так:
КЛАССИФИКАЦИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА
В Методическом руководстве по диагностике и лечению сахарного диабета, предиабета и сердечно-сосудистых заболеваний, разработанном Европейским кардиологическим обществом (ESC) совместно с Европейской ассоциацией по изучению сахарного диабета (EASD) в 2007 г. приведены три варианта идентификации метаболического синдрома: в соответствии с рекомендациями ВОЗ (1998), Adult Treatment Panel III (ATP-III, 2001) и Международной Федерации по изучению СД (IDF, 2005).
1. Критерии метаболического синдрома, рекомендуемые ВОЗ:
2. Критерии метаболического синдрома, рекомендуемые ATP III (Adult Treatment Panel III или Третьего отчета группы экспертов по выявлению, оценке и лечению гиперхолестеринемии у взрослых в рамках Национальной образовательной программы США/NCEP/пo ХС):
а наличие избыточной массы тела и ожирения связывают с резистентностью к инсулину и метаболическим синдромом. Тем не менее, ожирение по абдоминальному типу в большей степени коррелирует с метаболическим синдромом, чем повышенный ИМТ. Поэтому обычное измерение окружности талии рекомендуется для выявления «весового» компонента метаболического синдрома;
b у некоторых пациентов мужского пола могут развиваться множественные метаболические факторы риска, если окружность талии погранично увеличена (например, 94–102 см/37–39 дюймов). Такие больные могут иметь значительную генетическую предрасположенность к развитию инсулинорезистентности. Коррекция образа жизни обеспечивает таким пациентам значительное преимущество;
с Американской ассоциацией по изучению сахарного диабета (ADA) недавно установлен предельный уровень, составляющий 5,6 ммоль/л или 100 мг/дл, превышение которого свидетельствует о наличии предиабета — нарушения толерантности к глюкозе, или сахарного диабета. Этот новый предельный уровень может быть использован для установления более низкой границы определения уровня глюкозы как одного из критериев метаболического синдрома.
3. Критерии метаболического синдрома, рекомендуемые Международной федерацией по изучению СД (IDF):
Кроме классического представления о метаболическом синдроме, изложенного в трех перечисленных выше документах, в 1997 г. C. Spencer и соавторами была выдвинута концепция менопаузального метаболического синдрома. На основании тщательного анализа работ, посвященных влиянию менопаузы на чувствительность к инсулину, показатели липидного и углеводного обмена, распределение жировой ткани и систему гемостаза, а также данных о влиянии заместительной гормональной терапии на перечисленные параметры у женщин, предложено выделять менопаузальный метаболический синдром как патогенетический комплекс факторов риска сердечно-сосудистых заболеваний, и в первую очередь ИБС, в основе которого лежит дефицит эстрогенов.
ЭПИДЕМИОЛОГИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ МЕТАБОЛИЧЕСКОГО СИНДРОМА
В начале третьего тысячелетия для человечества, преодолевшего на протяжении многовековой истории эпидемии жизненно опасных инфекций, на 1-е место по актуальности среди всех причин заболеваемости и смертности вышла проблема сердечно-сосудистых заболеваний. Значительную роль в этом сыграла модификация образа жизни, связанная с ограничением физической активности, повышением калорийности пищевых продуктов и неустанным ростом эмоционально-стрессовых нагрузок. Все это потенцировало основные модифицируемые факторы риска возникновения сердечно-сосудистых заболеваний, ставшие отрицательным достоянием прогресса, такие как: повышение АД, дислипидемии, сахарный диабет и ожирение. С 1988 г. после Бантинговской лекции G.Reaven взаимосвязанное сочетание данных патологий принято обозначать единым термином «метаболический синдром Х».
Основная идея создания концепции метаболического синдрома заключается в выделении популяции пациентов с высоким кардиоваскулярным риском, у которых проведение профилактических мероприятий, включающих модификацию образа жизни и применение адекватных лекарственных средств может значимо повлиять на основные показатели здоровья. Выделение пациентов с метаболическим синдромом имеет также большое клиническое значение, поскольку, с одной стороны, это состояние является обратимым, то есть при соответствующем лечении можно добиться исчезновения или, по крайней мере, уменьшения выраженности основных его проявлений, с другой — оно предшествует возникновению такой патологии, как сахарный диабет II типа и атеросклероз, что неразрывно связано с повышением смертности в популяции.
Установлено, что у больных АГ с ожирением риск развития ИБС повышен в 2–3 раза, а риск инсульта — в 7 раз. По результатам Фремингемского исследования отмечено, что как САД, так и ДАД повышалось в среднем на 1 мм рт.ст при увеличении массы тела на 1 кг.
Степень кардиоваскулярного риска при ожирении зависит от распределения жировой ткани в организме и значительно выше при так называемом центральном или андроидном типе, то есть при расположении жира преимущественно в области туловища по сравнению с бедрами и ягодицами. У пациентов с ожирением отмечают увеличение сердечного выброса с целью восполнения возросших метаболических потребностей, которое достигается не за счет повышения ЧСС, а за счет увеличения ударного объема. Высокий сердечный выброс ведет к развитию эксцентрической ГЛЖ и диастолической дисфункции. Если же утолщение стенки желудочка происходит несинхронно с дилатацией его полости, то создаются условия для формирования систолической дисфункции с последующим развитием кардиомиопатии ожирения и застойной СН на фоне увеличения внутрисосудистого объема. Предшествование или присоединение к клинической картине АГ усугубляет прогрессирование структурно-функциональных нарушений в миокарде. Формирование же ГЛЖ является самостоятельным предиктором развития внезапной смерти, причем, по данным Фремингемского исследования, половина мужчин старше 45 лет с ЭКГ-признаками ГЛЖ умирала в последующие 8 лет.
Известно, что адипоциты висцеральной жировой ткани секретируют свободные жирные кислоты, попадающие в воротную вену печени. Высокие концентрации свободных жирных кислот подавляют поглощение инсулина печенью, что приводит к гиперинсулинемии и относительной инсулинорезистентности, что сочетается с гипергликемией и гипертриглициридемией. В свою очередь, гиперинсулинемия приводит к развитию АГ посредством усиления реабсорбции натрия в нефронах и задержки жидкости; стимуляции САС; повышения содержания внутриклеточного кальция и ремоделирования артерий с утолщением их медии. Согласно современным представлениям, объединяющей основой всех проявлений метаболического синдрома являются первичная инсулинорезистентность и сопутствующая системная гиперинсулинемия. При этом инсулинорезистентность — это снижение реакции инсулинчувствительных тканей на инсулин при его достаточной концентрации. Наличие сахарного диабета значительно усиливает патогенное влияние основных факторов риска и предъявляет более жесткие требования к максимально допустимым величинам АД, с другой стороны, контроль АД, гиперлипидемии и гипергликемии положительно отражается на прогнозе жизни больного.
Как уже упоминалось, наиболее патогенным в развитии метаболического синдрома является абдоминальный тип ожирения. КТ и МРТ позволили изучить особенности распределения жира при абдоминальном ожирении. На основании полученных данных жировую ткань разделяют на висцеральную (интраабдоминальную) и подкожную. Именно повышение количества висцерального жира, как правило, сочетается с гиперинсулинемией, инсулинорезистентностью, АГ и липидными нарушениями. Строение висцеральной жировой ткани характеризуется морфологическими и функциональными особенностями. Интраабдоминальные адипоциты имеют большую плотность β-адренорецепторов, кортикостероидных и андрогенных рецепторов и относительно меньшую плотность α2-адренорецепторов и рецепторов к инсулину. Это определяет высокую чувствительность висцеральной жировой ткани к липолитическому действию катехоламинов и низкую — к антилиполитическому действию инсулина. Интенсивный липолиз в интраабдоминальных адипоцитах приводит к высвобождению большого количества свободных жирных кислот, которые поступают по воротной вене в печень, а затем в системный кровоток. Печень подвергается мощному и постоянному воздействию свободных жирных кислот, что приводит к целому ряду метаболических нарушений, развивается инсулинорезистентность, а затем системная гиперинсулинемия.
Свободные жирные кислоты в печени утилизируются двумя путями: либо активируют глюконеогенез, способствуя увеличению продукции глюкозы и снижению активности фосфатидил-нозитол-3-киназы инсулинового рецептора, нарушая транспорт глюкозы внутрь клеток, что приводит к развитию гипергликемии (эффект липотоксичности); либо используются для синтеза ТГ. Характер распределения жировой ткани оценивают с помощью отношения окружности талии к окружности бедер (ОТ/ОБ) пациента, измеренных с помощью сантиметровой ленты. При наличии абдоминального ожирения этот показатель превышает 1,0 у мужчин и 0,8 у женщин. Распределение жировой ткани в теле человека подвержено генетическому контролю.
Возникающая благодаря избыточному накоплению адипозной ткани инсулинорезистентность служит связующим звеном между ожирением, нарушением толерантности к глюкозе, АГ и дислипидемией.
Следует указать, что предрасположенность к инсулинорезистентности — это исторически сложившийся механизм адаптации организма человека к изменению внешних условий для поддержания энергетического баланса и нормального функционирования всех органов и систем. Для объяснения этой генетической предрасположенности к инсулинорезистентности J. Neel в 1962 г. выдвинул теорию бережливого генотипа. Согласно этой теории организм человека во времена благополучия и достатка в питании накапливал жиры и углеводы, а в периоды дефицита пищи сохранял нормогликемию и более экономно расходовал энергию за счет снижения уровня утилизации глюкозы в мышечной ткани, усиления глюконеогенеза и липогенеза. Таким образом, инсулинорезистентность способствовала выживанию человека в периоды голода. Инсулинорезистентность в течение определенного времени поддерживает организм в состоянии между здоровьем и болезнью. Однако сегодня в условиях гиподинамии и хронического переедания жиров, а также при наличии других неблагоприятных факторов, этот механизм становится патологическим и приводит к развитию сахарного диабета II типа, АГ, атеросклероза (Himsworth H., 1936; Reaven G., 1988; Warram J. и соавт., 1990).
В современной литературе принято указывать, что в 1988 г. G. Reaven ввел термин «синдром Х» или «метаболический синдром», критерии которого были уточнены в 2001 г. в рекомендациях Национального института здоровья США, и который нередко называют также смертельным квартетом, поскольку он подразумевает:
Однако рассмотрение проблемы метаболического синдрома началось значительно раньше. В 1966 г. J. Camus предложил проанализировать взаимосвязь между развитием гиперлипидемии, сахарного диабета II типа и подагры. Подобный вид нарушений обмена он назвал метаболический трисиндром (trisyndrome metabolique). В 1968 г. Н. Mehnert и Н. Kuhlmann описали взаимосвязь факторов, приводящих к обменным нарушениям при АГ и сахарном диабете, и ввели понятие «синдром изобилия». Позднее, в 1980 г., M. Henefeld и W. Leonhardt подобный вид нарушений стали описывать как метаболический синдром. А уже в конце 1980-х годов несколько авторов (Christlieb A.R. et al., 1985; Modan М. et al., 1985; Landsberg L., 1986; Ferranini Е. et al., 1987; Lithell Н. et al., 1988) независимо друг от друга отметили взаимосвязь между развитием у пациентов артериальной гипертонии, гиперлипидемии, инсулинорезистентности и ожирения.
И лишь в 1988 г. G. Reaven в своей Бантинговской лекции, впоследствии опубликованной в журнале «Diabetes», предложил термин «синдром X», в который включал тканевую инсулинорезистентность, гиперинсулинемию, нарушение толерантности к глюкозе, гипертриглицеридемию, снижение ХС ЛПВП и АГ. После чего в 1989 г. N. Kaplan показал, что у большинства пациентов с этим синдромом отмечают центральное ожирение, а для развернутой клинической картины данного вида метаболических нарушений предложил термин «смертельный квартет» (ожирение, АГ, сахарный диабет, гипертриглицеридемия). Позже был выявлен целый ряд состояний, которые ассоциируются с синдромом инсулинорезистентности: ГЛЖ с нарушением диастолической дисфункции, повышение внутрисосудистой свертываемости крови и др. В настоящее время наиболее употребляемым термином является «метаболический синдром». Учитывая ведущий патогенетический механизм его развития, нередко в качестве синонима используют термин «синдром инсулинорезистентности».
Золотым стандартом выявления инсулинорезистентности является эугликемическая клэмп-методика с использованием биостатора. Суть ее заключается в том, что пациенту в вену одновременно вводят растворы глюкозы и инсулина. Причем количество инсулина постоянное, а глюкозы — меняется для того, чтобы поддерживать определенный (нормальный) уровень глюкозы в крови. Значения вводимой глюкозы оценивают в динамике. Скорость введения глюкозы отражает биологическую эффективность инсулина. Определение инсулинорезистентности этим методом возможно лишь при наличии соответствующего оборудования. Косвенными показателями инсулинорезистентности можно считать:
M.N. Duncan и соавторы установили, что также можно использовать индекс инсулинорезистентности = (гликемия натощак)·(базальный уровень иммунореактивного инсулина):25.
Повышенное поступление свободных жирных кислот в печень и инсулинорезистентность гепатоцитов приводят к повышению синтеза ТГ и ЛПОНП. При инсулинорезистентности снижается активность липопротеидлипазы, которая контролируется инсулином. Возникает характерный тип дислипидемии, связанный с висцеральным ожирением: повышение концентрации ЛПОНП и ТГ, снижение концентрации ЛПВП и увеличение количества мелких плотных частиц ЛПНП. Таким образом, ожирение и инсулинорезистентность способствуют развитию нарушений липидного профиля, которые наряду с гипергликемией и гипертензией приводят к более раннему и быстрому развитию атеросклероза у больных с нарушениями углеводного обмена и висцеральным ожирением.
По результатам Фремингемского исследования, увеличение массы тела на 10% сопровождалось повышением концентрации ХС в плазме крови на 0,3 ммоль/л.
В то же время, сама концепция метаболического синдрома как кластера факторов риска сахарного диабета и кардиоваскулярных заболеваний претерпела за истекшие годы ряд эволюционных преобразований. До 2005 г. согласно рекомендациям АНА и Европейского общества кардиологов, верификацию метаболического синдрома производили в соответствии с критериями, изложенными в 2001 г. в программе АТР-III. Однако полученные в последнее время данные внесли существенные коррективы в профилактическую концепцию метаболического синдрома. Новая редакция определения метаболического синдрома была представлена в апреле 2005 г. на I Международном конгрессе по предиабету и метаболическому синдрому в Берлине, проводившемся Международной федерацией по сахарному диабету и на 75-м конгрессе Европейского общества по атеросклерозу в Праге.
Основной мотивацией для выдвижения нового консенсуса по метаболическому синдрому стало желание примирить специалистов с различными точками зрения; определить объединенный рабочий диагностический алгоритм и подчеркнуть те области, где больше необходимо накопление научных знаний. Принципиально новой позицией было утверждение абдоминального ожирения как основного критерия диагностики метаболического синдрома с ужесточением нормативных параметров объема талии ( 5,6 ммоль/л). При этом еще раз было подчеркнуто, что макрососудистые осложнения (ИБС, ИМ, церебральный инсульт) являются главной причиной смерти больных с метаболическим синдромом и сахарным диабетом. Риск развития смерти больного с метаболическим синдромом без клинических проявлений коронарной недостаточности вследствие основных сердечно-сосудистых осложнений такой же, как у больных, ранее перенесших ИМ без метаболического синдрома на момент включения в исследование. Кроме того, еще раз была подчеркнута необходимость адекватности выбора патогенетически обоснованного антигипертензивного лечения, способного защитить органы-мишени, поскольку именно контроль АД является первостепенной задачей для терапии данного контингента больных, позволяя на 51% уменьшить количество основных кардиоваскулярных событий, в то время как контроль гиперлипидемии снижает риск смерти от ИБС — на 36%, а коррекция уровня гипергликемии может снизить частоту развития ИМ только на 16%.
Следует отметить, что единой концепции метаболического синдрома для лиц мужского и женского пола не существует, поскольку формирование метаболического синдрома у мужчин находится в прямой зависимости от выраженности абдоминального ожирения, а у женщин такая зависимость от ожирения появляется только с наступлением менопаузы и гипоэстрогенемии. Менопаузальный метаболический синдром мы сознательно выделяем потому, что 50% пациентов с АГ составляют женщины в период менопаузы, частота выявления сахарного диабета II типа у женщин 40–50 лет — 3–5%, а в возрасте 60 лет — 10–20%, то есть с возрастом прогрессируют нарушения углеводного обмена.
Различие степени риска возникновения фатальных сердечно-сосудистых заболеваний нашло свое отражение в системе SCORE, презентованной еще в 2003 г. на конгрессе Европейского общества кардиологов. Оно свидетельствует о том, что у мужчин сердечно-сосудистые заболевания начинают прогрессировать с достижением 40-летнего возраста, тогда как у женщин такая закономерность возникает лишь с достижением возраста 50–55 лет и наступлением менопаузы.
В исследовании DECODE установлено, что повышение АД и нарушение чувствительности к инсулину повышают риск развития сердечно-сосудистых заболеваний у женщин в постменопаузальный период даже при незначительных изменениях АД и чувствительности к инсулину. Наиболее уязвимый период переходного возраста женщин — пременопауза, то есть начальный период снижения функции яичников (в основном в возрасте старше 45 лет и до наступления менопаузы), что сопровождается критическим снижением уровня эстрогенов. Реализация дефицита эстрогенов в период менопаузы включает влияние на метаболизм липопротеинов, прямое влияние на биохимические процессы в стенке сосудов через специфические рецепторы к эстрогенам, а также опосредованное влияние через метаболизм глюкозы, инсулина, гомоцистеина, систему гемостаза и т.д.
Логическим продолжением таких взглядов стала презентация гипотезы о гендерном различии в патогенезе метаболического синдрома у мужчин и женщин в рамках секционных заседаний «Женщины в сердце» в сентябре 2005 г. на очередном Конгрессе европейского общества кардиологов. Основная идея этой гипотезы бази руется на постулате о том, что у мужчин ведущим предиктором метаболического синдрома является абдоминальное ожирение независимо от возраста; у женщин основные пусковые механизмы формирования метаболического синдрома — сахарный диабет и менопауза. Высказана мысль о том, что менопауза — это естественная модель иммунорезистентного состояния и эндотелиаль ной дисфункции.
КЛИНИКА И ДИАГНОСТИКА МЕТАБОЛИЧЕСКОГО СИНДРОМА, САХАРНОГО ДИАБЕТА И ПРЕДИАБЕТА
Неуклонное прогрессирование всемирной эпидемии сахарного диабета и метаболического синдрома не оставило равнодушными большинство практикующих врачей, пришедших к заключению, что только полисистемный подход к решению этой задачи может увенчаться успехом. Сахарный диабет и заболевания сердечно-сосудистой системы часто представляют собой две стороны одной медали: с одной стороны, сахарный диабет можно расценивать как состояние, способствующее развитию ИБС, а с другой — у многих пациентов с уже существующей ИБС отмечают сахарный диабет или предиабетическое состояние. Таким образом, давно назрела необходимость выработать совместный подход к этой проблеме со стороны кардиологов и эндокринологов, что позволит повысить качество диагностики и лечения в рамках единой медицинской помощи миллионам пациентов с сердечно-сосудистыми и метаболическими заболеваниями.
Подобный кардиодиабетологический подход не только крайне важен для пациентов, но и открывает путь для дальнейшего прогресса в области кардиологии и диабетологии. Европейское кардиологическое общество (ESC) и Европейская ассоциация по изучению сахарного диабета (EASD), отвечая на этот призыв, приняли решение о разработке объединенных, основанных на принципах доказательной медицины, рекомендаций по лечению сахарного диабета и сердечно-сосудистых заболеваний. Цель внедрения данных рекомендаций заключается в улучшении лечебно-профилактической помощи пациентам с манифестным сахарным диабетом, больным с нарушенной толерантностью к глюкозе и высоким риском развития сахарного диабета, а также в повышении эффективности терапии сердечно-сосудистых заболеваний в данной популяции.
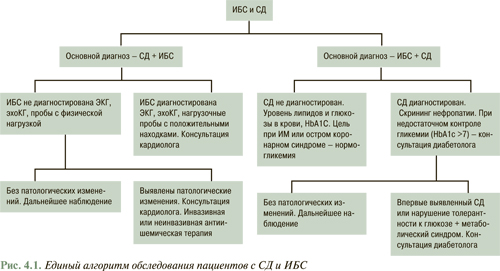
В рекомендациях были приняты классы рекомендаций и уровни доказательности для оценки терапевтических подходов, ставшие уже традиционными для большинства подобных методических руководств. Суть единого подхода рабочей группы к рассматриваемой проблеме выражена в рис. 4.1.
Краеугольный камень терапии любого из патологических состояний — установление диагноза и выбор наиболее адекватной терапии. Для этого необходимым будет знакомство кардиологов с каноническим для диабетологов подходом для верификации основного диагноза в соответствии с критериями ВОЗ (1999) и Американской ассоциации по диабету (ААД) (1997, 2003) (табл. 4.1)