Дисфункция сфинктера Одди
Введение
Определение
Билиарная ДСО
Следует отметить, что в клинической практике преобладают пациенты 3й группы.
Панкреатическая ДСО
Диагностика
Считается, что «золотым стандартом» диагностики ДСО является манометрия сфинктера Одди [13]. Выполняется манометрия во время РХПГ с помощью специального баллона. Определяется базовый тонус сфинктера и его фазовые сокращения. Патологическим считается давление выше 40 мм водного столба. К другим патологическим признакам относят повышенную частоту волновых сокращений, увеличения числа ретроградных перистальтических волн [12]. Отсутствие снижения давления сфинктера при введении гладкомышечных релаксантов (нитраты, блокаторы кальцевых каналов) так же имеет диагностическое значение. Однако повышенное давление в сфинктере Одди выявляется при билиарной форме в 86 % случаев в 1й группе, примерно в 55 % случаев во второй группе и у 28 % больных третьей группы (билиарный тип) и при панкреатической форме ДСО в 92 %, 58 %, 35 % больных соответственно [4]. Таким образом приходиться признать, что хотя бы у части больных с характерной клиникой постоянного гипертонуса сфинктера не наблюдается. К сожалению метод манометрии в нашей стране малодоступен, дорог и кроме того, ее выполнение связанно с определенным риском развития панкреатита. Что мы можем использовать в реальной клинической практике?
УЗИ. Выполнение УЗИ после назначения пациенту завтрака с высоким содержанием жира (что стимулирует выделение желчи) у пациентов с ДСО приводит к дилатации холедоха в результате повышения в нем давления из-за нарушения оттока. Диагностическим считается увеличение диаметра более чем на 2 мм при измерении его через 45 минут после завтрака. Метод легко доступен практически в любом лечебном учреждении. Его специфичность достигает 97 %, однако чувствительность только 21 % (сравнение проводилось с манометрией) [10]. Кстати, вместо завтрака можно использовать стимуляцию холецистокинином, а для исследования панкреатического протока серетином.
Существуют сообщения об успешном использовании синцитографии для диагностики ДСО. Однако методика достаточно сложна, да и специфичность с чувствительностью составляют 78 % и 49 % соответственно [10].
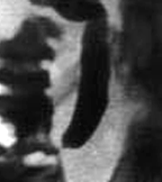
В нашей практике мы в основном используем УЗИ. Кроме того, при выполнении таким больным РХПГ и выявленной стриктуре терминального отдела холедоха или просто замедлении опорожнения желчных путей пациенту даются нитраты. Начало (или ускорение) их опорожнения после введения нитратов по нашему мнению с определенной степенью уверенности позволяет говорить о наличии у больного ДСО. Этот тест в определенной степени помогает дифференцировать анатомические и функциональные изменения сфинктера. В ряде случаев, казалось бы, явные стриктуры терминального отдела холедоха полностью исчезали поле применения нитратов, рубцовые сужения на введение препаратов не реагировали. На рисунках показана типичная для пациентов ДСО картина РХПГ (сужение в терминальном отделе общего желчного протока).
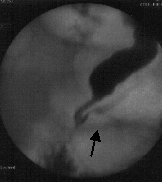
Выявленный на РХПГ билиарно-панкреатический рефлюкс так же позволяет заподозрит эту патологию, особенно при наличии у пациента клиники идиопатического рецидивирующего панкреатита. Картина рефлюкса предтавлена на следующм рисунке.
Лечение
Эндоскопическая сфинктеротомия (ПСТ). Это весьма эффективное вмешательство значительно облегчающее жизнь больных при условии правильного отбора пациентов. Она абсолютно показана больным 1й группы и пациентам 2-3 групп, при условии повышенного базального давления сфинктера Одди. Такой вывод был сделан на основании исследования эффективности ПСТ у больных разных групп. Так у пациентов 1й группы положительный эффект от сфинктеротомии наблюдается в подавляющем большинстве случаев и, что интересно, наблюдался даже у пациентов этой группы с нормальным базальным давлением в сфинктере [9]. У больных 2й группы и с повышенным базальным давлением в сфинктере Одди ПСТ приводила к положительному клиническому результату в примерно 90 % наблюдений, при отсутствии этого критерия вмешательство было малоэффективно [3]. Geenen J.T. et al., рандомизировал пациентов с повышенным и нормальным давлением в сфинктере на ПСТ и «ложную» ПСТ. Процент пациентов с улучшением после настоящей и ложной ПСТ в группе с нормальным давлением существенно не различались (42 % и 33 % соответственно), тогда как у больных с давлением выше 40 мм водного столба сфинктеротомия приводила к гораздо более высокому проценту клинического улучшения, чем ее имитация (91 % и 25 % соответственно) [3]. У пациентов 3й группы наблюдается наименьшая результативность ПСТ, даже при условии повышенного давления в сфинктере [13]. Т.к. мы в своей работе возможности измерения давления решены, то во 2й группах мы выполняем ПСТ при выявлении на РХПГ стриктур или замедлении опорожнения холедоха, а так же пациентам этой группы с неэффективной медикаментозной терапией и выраженным болевым синдромом. Больным 3й группы ПСТ мы стараемся не выполнять (учитывая, что в этой группе процент случаев повышенного базального давления в сфинктере Одди мал и, следовательно, лишь небольшая часть пациентов выиграет от выполнения ПСТ, кроме того, у них более высок риск развития панкреатита и меньшая эффективность ПСТ). Что касается панкреатической формы ДСО, то ПСТ мы выполняем только в случае выявления билиарно-панкреатического рефлюкса.
Хирургическую сфинктеротомию, сфинктеропласику и иссечение сфинктера, описанные в качестве лечения ДСО мы в своей практике не применяли. В любом случае, только манометрические данные, точно верифицирующие ДСО и неэффективность всех вышеописанных методов могут оправдывать такие высоко инвазивные вмешательства.
Введение ботулинового токсина в сфинктер может быть результативным у ряда пациентов [14]. Однако вопрос степени и продолжительности положительного эффекта остается пока открытым.
Заключение
Конечно, проблема ДСО весьма сложна и далека от своего решения. Необходимо разработать неинвазивные, простые, дешевые и достоверные методы диагностики, эффективное медикаментозное лечение. Здесь были изложены как общемировые подходы к диагностике и лечению данной патологии, так и наши собственные мысли по решению данной проблемы (о правильности последних судить Вам).
Спазм сфинктера Одди
Рубрика МКБ-10: K83.4
Содержание
Определение и общие сведения [ править ]
Дисфункция сфинктера Одди проявляется нарушением тонуса сфинктера ОЖП (общего желчного протока), главного панкреатического протока (ГПП) или общего сфинктера. Моторная активность сфинктера Одди рефлекторно связана с активностью желчного пузыря, так как тонус сфинктера уменьшается во время сокращения желчного пузыря, что и обеспечивает координированную работу билиарной системы. Кроме того, желчный пузырь модулирует ответ сфинктера Одди на гормональную регуляцию. Нарушение моторной функции сфинктера после холецистэктомии может быть одной из причин абдоминальных болей и диспепсических явлений в послеоперационный период.
Дисфункцию сфинктера Одди обнаруживают у 1% больных, перенесших холецистэктомию, и у 14% больных, предъявляющих жалобы, характерные для постхолецистэктомного синдрома.
Гипертонические расстройства сфинктера Одди в панкреатическом сегменте также разделяют на три типа.
1-й тип панкреатической дисфункции сфинктера Одди (определенный)
К этой группе относят больных с идиопатическим рецидивирующим панкреатитом или типичными панкреатическими болями при повышении уровня амилазы/липазы в 2 раза выше нормы (двукратно или более), расширенным протоком ПЖ (>5 мм) и увеличенным временем поступления секрета по панкреатическому протоку (>10 мин).
2-й тип панкреатической дисфункции сфинктера Одди (предположительный)
Больные из этой группы имеют типичные панкреатические боли и один или два критерия из первого типа.
3-й тип панкреатической дисфункции сфинктера Одди (возможный)
Больные этой группы жалуются на панкреатические боли, но не имеют каких-либо расстройств, подтвержденных объективно (вирсунгодискинезия).
Пациенты с 1-м типом расстройств сфинктера Одди имеют структурные нарушения самого сфинктера или зоны фатерова сосочка (склероз); у больных со 2-м и 3-м типом выражены также и так называемые функциональные нарушения.
Этиология и патогенез [ править ]
Причиной дисфункции сфинктера Одди после холецистэктомии считают структурные нарушения (часто стеноз), или мышечную дискинезию. Мышечная дискинезия сфинктера Одди наиболее часто проявляется гипертонусом сфинктера. Холецистэктомия в первые несколько месяцев после операции нередко сопровождается временным усилением тонуса сфинктера Одди.
Нарушения функции сфинктера Одди и механизм развития боли при ДСО заключаются в развитии спазма сфинктерных мышечных волокон и повышении давления в системе желчных протоков или протока ПЖ. Конкретные факторы, вызывающие длительные спазмы сфинктера Одди, неизвестны. Вероятно, к ним можно отнести дуоденит, воспаление вокруг или в самом большом сосочке ДПК (папиллит или фиброз). Получены данные, указывающие на особые повреждения неадренергических нехолинергических ингибирующих нейронов.
Клинические проявления [ править ]
Для гипокинетического и гипотонического варианта дисфункции типичны тупые боли в правом подреберье, чувство давления, распирания, усиливающиеся при наклоне туловища, с появлением тошноты, горечи во рту, метеоризма. Данную форму чаще выявляют у лиц, склонных к запорам и ожирению.
Спазм сфинктера Одди: Диагностика [ править ]
При клинических симптомах дисфункции сфинктера Одди необходимо провести УЗИ билиарного тракта, выполнить печеночные пробы, измерить уровень активности панкреатических ферментов. Если результаты проведенных исследований в пределах нормы, то выполняют ФЭГДС (фиброэзофагогастродуоденоскопия). Основной задачей при диагностике дисфункции сфинктера Одди должно быть исключение структурных изменений в зоне сфинктера, которые могут послужить причиной затруднения оттока желчи и сока ПЖ.
«Золотым стандартом» в распознавании дисфункции сфинктера Одди считают манометрию сфинктера Одди (с раздельным канюлированием желчного и панкреатического сегментов). Диагностически значимым считают повышение уровня базального давления в сфинктере более 35 мм рт.ст. Кроме того, фиксируют другие нарушения двигательной функции: высокочастотные фазовые сокращения (тахиоддию), обширные ретроградные сокращения, парадоксальный ответ на холецистокинин.
Диагностические исследования, уточняющие состояние сфинктера Одди
• Определение в крови активности аминотрансфераз, щелочной фосфатазы, билирубина, амилазы, липазы.
•ЭРХПГ (эндоскопическая ретроградная холангиопанкреатография).
• Манометрия сфинктера Одди
Дифференциальный диагноз [ править ]
1. Некалькулезный холецистит. Мужчины старше 55 лет, пациенты с тяжелыми сопутствующими заболеваниями: множественными травмами, повторными операциями, сахарным диабетом, инфарктом миокарда, полиорганной недостаточностью и др. Доминирует основное заболевание, билиарная колика имеет стертое течение, необъяснимый сепсис. Лейкоцитоз, в 1,5-2 раза повышение активности АСТ, АЛТ, ЩФ, концентрации билирубина.
2. Постхолецистэктомический синдром. Состояния, обусловленные техническими погрешностями операции (гемобилии, травматическая рубцовая стриктура общего желчного протока, оставленная патологическая культя пузырного протока, неустраненный холедохолитиаз, неликвидированный стеноз сфинктера Одди и др.).
Спазм сфинктера Одди: Лечение [ править ]
Показано соблюдение диеты с исключением жирной, острой пищи, сырого лука и чеснока, алкоголя, приправ, томатного сока, обильного приема пищи. Рекомендуют частое дробное питание (5-6 раз в день).
Изменение образа жизни: нормализация массы тела, отказ от курения, исключение чрезмерных физических нагрузок (например, бега).
Для снятия спазма гладкой мускулатуры сфинктера Одди используют нитраты, антихолинергические средства, блокаторы медленных кальциевых каналов и миотропные спазмолитики (папаверин внутрь по 40-60 мг, пинаверия бромид внутрь 50 мг, дротаверина внутрь 40-80 мг, мебеверин внутрь 200-400 мг 2 раза в сутки в течение 1-2 мес). Задача фармакотерапии спазма сфинктера Одди состоит в выборе фармакологического средства, избирательно воздействующего на билиарную систему и вызывающего минимум побочных эффектов. Имеющиеся данные свидетельствуют, что мебеверин обладает избирательным действием в отношении сфинктера.
Неселективные блокаторы медленных кальциевых каналов (нифедипин, верапамил и др.) способны расслабить гладкую мускулатуру, в том числе и желчевыводящих путей, но это требует максимально высоких доз, что практически исключает использование данных препаратов из-за выраженных кардиоваскулярных эффектов.
Препарат гимекромон (принимают внутрь по 200-400 мг 3 раза в сутки перед едой в течение 1-2 мес) оказывает избирательное спазмолитическое действие на сфинктер Одди и сфинктер желчного пузыря. Он эффективен у пациентов с дисфункцией желчевыводящих путей, обладает желчегонным действием, устраняет билиарную недостаточность, а также дисфункцию сфинктера Одди, его гипертонус, в том числе и у больных после холецистэктомии.
Показания для сфинктеротомии следующие:
• Рецидивирующие панкреатиты, при которых отмечают положительный эффект от введения стента в панкреатический проток
• Отсутствие эффекта от консервативной терапии дисфункции сфинктера Одди, если испробованы все медикаментозные варианты
Эффективность папиллосфинктеротомии стеноза сфинктера Одди достигает 90%. Использование ботулинического токсина в виде инъекций в сфинктер уменьшает его давление, улучшает ток желчи и приносит облегчение, но эффект лечения неустойчивый. При панкреатическом типе дисфункции сфинктера Одди стандартной терапией считают оперативную сфинктеропластику.
Спазм сфинктера Одди (K83.4)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Примечание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
1. Билиарный тип. В основу диагностических критериев положены:
1.1 Приступ болей билиарного типа.
1.2 Три лабораторно-инструментальных признака:
— подъем печеночных проб (ACT или ЩФ) в два раза и более при двукратном определении, с нормализацией в течение 48 часов;
— замедление выведения контрастных веществ при ЭРПХГ (более 45 минут);
— расширение общего желчного протока более 12 мм (исследования проводят в период приступа).
ЭРХПГ является инвазивным методом диагностики, который может иметь серьезные осложнения (воспаление протоков поджелудочной железы или повреждение ее тканей). В связи с этим Римским консенсусом III предложена модификация, использующая неинвазивные методы оценки (УЗИ), сопряженные с меньшими опасностями.
наличие всех других признаков
наличие одного из других признаков
билиарная боль
При билиарном типе 1 ДСО чаще всего наблюдаются структурные изменения самого сфинктера (стеноз).
При типе 2 нарушения могут быть как структурными так и функциональными.
При типе 3 дисфункция сфинктера Одди, как правило, функциональна.
— в головке поджелудочной железы > 6 мм,
— в теле железы > 5 мм
Этиология и патогенез
Эпидемиология
Признак распространенности: Распространено
Соотношение полов(м/ж): 0.5
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
— эпизоды болей продолжительностью не менее 6 месяцев до установления диагноза и проявляющиеся не менее 3 месяцев;
— продолжительность эпизодов болей 30 минут и более;
— рецидивы болей ( не ежедневные);
— интенсивность болей умеренная или сильная (вплоть до госпитализации);
— боль не уменьшается после стула, при перемене положения, после приема антацидов.
Таким образом, особенности клинической симптоматики дисфункций билиарного тракта выделяют их из всего ряда функциональной патологии, где ночная симптоматика является критерием исключения.
Диагностика
Показатели манометрии сфинктера Одди
| Показатели | Общий желчный проток (ОЖП) | Главный панкреатический проток (ГПП) | |
| Давление в протоке, мм рт.ст. | 7,4 ± 1,7 | 8,0 ± 1,6 | |
| Базальное давление, мм рт.ст. | 16,2 ± 5,8 (8-26) | 17,3±5,8 (8-26) | >40 |
| 136,5 ± 25,9 (82-180) | 127,5 ± 21,5 (90-160) | >350 | |
| Длительность фазовых волн, с | 4,7±0,9 (3-6) | 4,8±0,7 | |
| Частота фазовых волн, за 1 мин. | 5,7±1,4 (3-10) | 5,8±1,5 (3-10) | >7 |
| Антеградные | 55 (10-100) | 53 (10-90) | — |
| Одновременные | 34 (0-70) | 35 (10-70) | — |
| Ретроградные | 11 (0-40) | 12 (0-40) | >50 |




.gif)
.gif)
_200.gif) После реабсорбции вторичных желчных кислот происходит их конъюгация с глицином или таурином, и они также становятся компонентами желчи. Урсодезоксихолевая кислота (УДХК) — третичная желчная кислота не превышает 5% от всех желчных кислот организма человека и также образуется под действием ферментов микроорганизмов [13].
После реабсорбции вторичных желчных кислот происходит их конъюгация с глицином или таурином, и они также становятся компонентами желчи. Урсодезоксихолевая кислота (УДХК) — третичная желчная кислота не превышает 5% от всех желчных кислот организма человека и также образуется под действием ферментов микроорганизмов [13].